Энергетическая константа
Cтраница 2
На базе молекулярно-кинетических представлений выполнен расчет свободной энергии кристалла. Исследованы уравнения равновесия, определяющие атомный и спиновый порядки в зависимости от температуры, состава кристалла, энергетических констант, а также взаимную зависимость спинового и атомного упорядочений. Оценены критические температуры атомного и спинового упорядочений, установлена их концентрационная зависимость, а также зависимость критической температуры спинового упорядочения от степени дальнего атомного порядка. Последняя оказалась дробно-рациональной функцией с числителем - полиномом четвертой степени и знаменателем - квадратичной функцией по параметру дальнего атомного порядка. [16]
Полученные выше выражения (38.20), (38.24) и (38.21) непосредственно решают поставленную нами задачу определения фурье-компонент парных потенциалов деформационного взаимодействия. Именно эти фурье-компоненты, взятые в точках обратного пространства, отвечающих положениям структурных и сверхструктурных векторов обратной решетки, представляют собой энергетические константы, определяющие термодинамику твердого раствора. [17]
Коэффициенты выходов зависят от природы источника углерода и энергии, а также от биохимических особенностей данного микроорганизма; когда источник энергии и углерода подавляет рост, коэффициенты выхода зависят также и от его концентрации. В случае источника углерода и энергии с относительно высоким содержанием углерода ( по сравнению с другими элементами) и, следовательно, с высокой энергетической константой при аэробном окислении наблюдается нарушение равновесия между высвобождением энергии и потреблением углерода; это ограничивает максимальный коэффициент выхода биомассы. [18]
Изучен частный случай очень низких температур, когда почти все электроны проводимости спарены в бозоны Купера. Обоснована возможность перехода кристалла CsjCeo в сверхпроводящее состояние при появлении атомов рубидия и образовании кристалла CsiRbCai. Установлен критерий для энергетических констант кристалла, при которых возможен фазовый переход в сверхпроводящее состояние. [19]
Вслед за тем Р. Г. Гребенщиков, используя данные собственных термохимических определений и литературные данные, проводит широкий круг теоретических исследований в области кристаллохимической энергетики силикатов и близких классов соединений. Выполненные им расчеты теплот образования важнейших анионных группировок силикатов и многих близких тугоплавких соединений позволили выявить ранее неизвестные корреляции между энергетической прочностью и тугоплавкостью в гомологических рядах соединений. В качестве новой коррелятивной термодинамической характеристики гомологов Р. Г. Гребенщиковым вводится понятие об изокомпонентах энергии комплексной решетки. Эти работы позволили связать энергетические константы поликомпонентных соединений с реально существующими в их кристаллических решетках структурными группировками и привели к развитию представлений об основных критериях изоморфизма применительно к сложным поликомпонентным системам. [20]
Две из этих констанг vm и п можно назвать структурными, так как одна из них зависит от величины всей адсорбирующей поверхности, а другая - от средней ширины пор. Эти величины не измеряются в абсолютных единицах, но выражаются через размеры адсорбированных молекул; константа vm зависит от числа молекул, требующихся для покрытия всей по-ве [ Х поли мономолекулярным слоем; таким образом, поверхность адсорбента измеряется через площадь поперечного сечения адсорбированной молекулы. Константа п равна максимальному числу адсорбированных слоев, которое может поместиться в капилляре; поэтому ширина пор измеряется через толщину адсорбированной молекулы нормально к поверхности. Другие две константы с и g могут быть названы энергетическими константами, так как они зависят от теплот адсорбции последовательно расположенных слоев. [21]
Две из этих констант vm и п можно назвать структурными, так как одна из них зависит от величины всей адсорбирующей поверхности, а другая - от средней ширины пор. Эти величины не измеряются в абсолютных единицах, но выражаются через размеры адсорбированных молекул; константа vm зависит от числа молекул, требующихся для покрытия всей поверх я ют и мономолекулярным слоем; таким образом, поверхность адсорбента измеряется через площадь поперечного сечения адсорбированной молекулы. Константа п равна максимальному числу адсорбированных слоев, которое может поместиться в капилляре; поэтому ширина пор измеряется через толщину адсорбированной молекулы нормально к поверхности. Другие две константы с и g могут быть названы энергетическими константами, так как они зависят от теплот адсорбции последовательно расположенных слоев. [22]
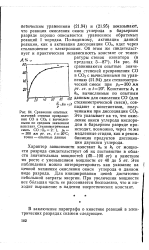 |
Сравнение опытных значений степени превращения СО в СО2 с вычисленными по средним значениям констант. Стехиометрическая смесь СО. О2 2. 1, ро 300 мм рт. ст., t 20 C. точки - опытные данные. [23] |
Характер зависимости констант & о и &i от мощности разряда свидетельствует об их постоянстве в области значительных мощностей ( 40 - 100 вт) и заметном их росте с уменьшением мощности от 40 до 5 вт. При увеличении мощности все большая часть ее рассеивается бесполезно, что и находит выражение в падении энергетических констант. [24]
Страницы: 1 2