Ступенчатая константа - устойчивость
Cтраница 2
Резкое изменение в величинах ступенчатых констант устойчивости объясняется перестройкой структуры комплекса, изменением состояния центрального иона или характера связи, пространственными затруднениями, что может также проявляться в необычных значениях энтальпии или энтропии образования комплекса [ 44; 67, гл. [16]
Выше указывалось, что если ступенчатые константы устойчивости kikj i, то всегда существуют такие интервалы равновесных концентраций лиганда, в которых имеет место равновесие только между двумя ионными формами исследуемого металла. [17]
У рассмотренных циа-нидных комплексов кадмия последовательные ступенчатые константы устойчивости отличаются не более чем на порядок, что и определяет совместное присутствие образующихся комплексов. [18]
Отношение вероятностей соответствует теоретическим отношениям ступенчатых констант устойчивости. Однако эксперимент не дает точного совпадения, и это указывает на влияние других факторов. [19]
Пользуясь справочником, приведите значения ступенчатых констант устойчивости ( IgKn) этих комплексов и сделайте вывод об устойчивости комплексов - реагентов и продуктов. [20]
Пользуясь справочникам, приведите значения ступенчатых констант устойчивости ( lg Кп) этих комплексов и сделайте вывод об устойчивости комплексов - реагентов и продуктов. [21]
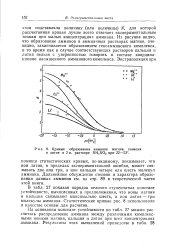 |
Кривые образования амминов магния, кальция и лития в 2 н. растворе NH4NO3 при 22 - 23. [22] |
В табл. 27 показан порядок величин ступенчатых констант устойчивости, вычисленных в предположении, что ионы магния и кальция связывают максимально шесть, а ион лития - три молекулы аммиака. [23]
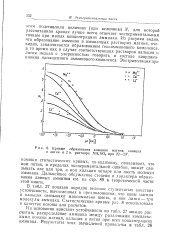 |
Кривые образования амминов магния, кальция и лития в 2 н. растворе NH4NO3 при 22 - 23. [24] |
В табл. 27 показан порядок величин ступенчатых констант устойчивости, вычисленных в предположении, что ионы магния и кальция связывают максимально шесть, а ион лития - три молекулы аммиака. [25]
В этом случае К и Kz обозначают ступенчатые константы устойчивости. [26]
В соответствии с принятыми обозначениями MII - ступенчатая константа устойчивости комплекса двухвалентного железа FeA 1, а и 1 - ступенчатая константа устойчивости комплекса трехвалентного железа FeA2; Pi2, Pin, Рзв2, Pis - общие константы устойчивости комплексов Fe ( III) составов FeAt, FeAOH, Fe3Ae ( OH) J и FeA3; Ka - константа протолитической диссоциации кислоты НА; Ю1 - [ FeOH ] fe / [ Fe3 l - константа гидролиза. [27]
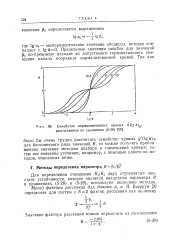 |
Семейство нормализованных кривых п ( lg а д, рассчитанных по уравнению ( 5 - 29. [28] |
Для определения отношения Ki / Kz двух ступенчатых констант устойчивости, которое является квадратом параметра R в уравнениях ( 5 - 28) и ( 5 - 29), используют несколько методов. [29]
На основе измерения ЭДС разработаны способы определения ступенчатых констант устойчивости при ступенчатом комплексооб-разовании ( И. [30]
Страницы: 1 2 3 4