Ассоциация - молекула - спирт
Cтраница 1
Ассоциация молекул спиртов вызвана водородной связью, возникающей между водородным атомом гидроксила одних молекул и кислородным атомом соседней молекулы за счет нзподеленных пар электронов кислородных атомов. [1]
Ассоциация молекул спирта через водородную связь объясняет низкое значение предэкспоненциального множителя реакции грег-бутилового спирта с озоном. [2]
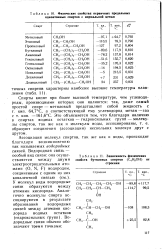 |
Физические свойства первичных предельных одноатомных спиртов с нормальной цепью.| Зависимость физических. [3] |
Ассоциация молекул спиртов, так же как и воды, происходит благодаря возникновению так называемых водородных связей. У молекул воды водородные связи образуются между атомами кислорода. [4]
Ассоциация молекул спиртов, так же как и воды, происходит благодаря возникновению так называемых водородных связей. Водородная связь - особый вид связи: она осуществляется между двумя электроотрицательными атомами ( О, N, F) водородом, соединенным с одним из них ковалентной связью ( стр. У молекул воды водородные связи образуются между атомами кислорода. [5]
Ассоциация молекул спирта и воды обусловлена образованием водородных связей. [6]
Такое резкое повышение температуры обусловлено значительной ассоциацией молекул спиртов. [7]
 |
Температуры кипения некоторых простых эфиров, алканов и спиртов. [8] |
Относительно высокая температура кипения спирта в каждой триаде, как считают, вызвана ассоциацией молекул спирта в жидкой фазе за счет межмолекулярных водородных связей, что не может происходить в случае простых эфиров или алканов, хотя в принципе эфиры могут принимать участие в образовании межмолекулярных водородных связей с протонсодержащими соединениями ( см. разд. Простые эфиры способны также образовывать комплексы с рядом кислот Льюиса, растворимые в эфирах же, они растворяют множество органических соединений и не вступают в реакции в широком диапазоне условий. Эти свойства делают простые эфиры весьма полезными растворителями для проведения органических реакций. Некоторые простые эфиры с низкой молекулярной массой, например диметиловый эфир или соединения с несколькими эфирными группами, например 1 2-диме-токсиэтан, растворимы в воде, однако высшие простые эфиры не смешиваются с водой и широко используются в органической химии для жидкостной экстракции. [9]
 |
Температуры кипения некоторых простых эфиров, алканов и спиртов. [10] |
Относительно высокая температура кипения спирта в каждой триаде, как считают, вызвана ассоциацией молекул спирта в жидкой фазе за счет межмолекулярных водородных связей, что не может происходить в случае простых эфиров или алканов, хотя в принципе эфиры могут принимать участие в образовании межмолекулярных водородных связей с протонсодержащнми соединениями ( см. разд. Простые эфиры способны также образовывать комплексы с рядом кислот Льюиса, растворимые в эфирах же, они растворяют множество органических соединений и не вступают в реакции в широком диапазоне условий. Эти свойства делают простые эфнры весьма полезными растворителями для проведения органических реакций. Некоторые простые эфиры с низкой молекулярной массой, например диметиловый эфир или соединения с несколькими эфирными группами, например 1 2-диме-токсиэтан, растворимы в воде, однако высшие простые эфиры не смешиваются с водой и широко используются в органической химии для жидкостной экстракции. [11]
Разница в физических свойствах связана с высокой полярностью гидроксильной группы, которая приводит к ассоциации молекул спирта за счет водородной связи ( см. гл. [12]
Это явление можно объяснить более резко выраженной водородной связью в гидроксильной группе, что способствует ассоциации молекул спирта и тем самым понижает их растворяющую способность. [13]
Это явление можно объяснить более резко выраженной водородной связью в гидроксильной группе, что способствует ассоциации молекул спирта и тем самым понижает их растворяющую способность. [14]
Как было показано ранее [3], основная трудность жидкофазного окисления первичных спиртов с использованием гомогенных катализаторов ( Со2 диацетил) связана с ассоциацией молекул спиртов. [15]
Страницы: 1 2