Кривая - заряжение
Cтраница 1
 |
Кривая заряжения пла. [1] |
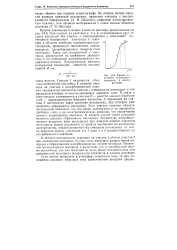
Кривая заряжения имеет три отчетливо выраженных участка: а, Ъ, с. [2]
 |
Кривая заряжения платинового электрода в кислом растворе. [3] |
Кривая заряжения платины в кислом растворе представлена на рис. 19.6. Она состоит из участков 1, 2 и 3, отличающихся друг от друга наклоном. На участке /, начинающемся у обратимого потенциала водородного электрода и лежащем в области наиболее отрицательных по-тенциалов, происходит постепенное снятие водорода, адсорбированного поверхностью злектрода. Здесь ток, подводимый к электроду, расходуется на заряжение двойного слоя и на ионизацию адсорбированных водородных атомов. [4]
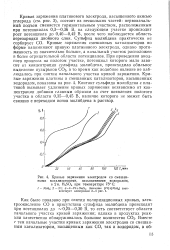 |
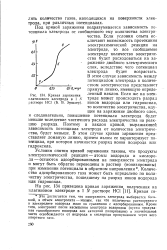
Кривые заряжения электродов со смешанными катализаторами, насыщенными водородом, в 2 н. H2SO4 при температуре 75 С. [5] |
Кривая заряжения платинового электрода, насыщенного окисью углерода ( см. рис. 3), состоит из нескольких частей: первоначальный подъем сменяется горизонтальным участком, расположенным при потенциалах 0 3 - 0 36 В, на следующем участке происходит рост потенциала до 0 40 - 0 42 В, после чего наблюдается область перезарядки двойного слоя. Сульфид молибдена практически не сорбирует СО. Кривые заряжения смешанных катализаторов по форме напоминают кривую платинового электрода, однако протяженность их значительно больше, а начальный участок расположен в более отрицательной области потенциалов. При проведении анодного процесса на пологом участке, потенциал которого мало зависит от концентрации сульфида молибдена, происходило обильное выделение пузырьков СО2, в то время как подобное явление не наблюдалось при снятии начального участка кривой заряжения. Контакт сульфида молибдена с платиной вызывает удлинение кривых заряжения независимо от концентрации добавки главным образом за счет появления пологого участка в области 0 35 - 0 45 В, наличие которого не может быть связано с переходом ионов молибдена в раствор. [6]
Кривой заряжения называют зависимость потенциала электрода Е от количества электричества AQ, сообщенного электроду. Наиболее удобно при измерении кривых заряжения для металлов группы платины использовать в качестве электрода сравнения обратимый водородный электрод в том же растворе. [7]
 |
Кривая заряжения ленный наклон. Если же на элек-платинового электрода в 1 N троде может происходить разряд растворе НС1 ( Б. В. Эршлер. ионов водорода или гидроксила. [8] |
Под кривой заряжения подразумевается зависимость потенциала электрода от сообщенного ему количества электричества. [9]
Из кривой заряжения может быть рассчитана также зависимость поверхностной концентрации атомарного водорода Лн от потенциала. [10]
На кривой заряжения после промывания Pt / Pt-элек-трода от метанола ( кривая / рис. 2) имеются две задержки; одна из них а отвечает окислению адсорбированного водорода, другая Ь - окислению прочно хе-мосорбированного вещества. На потенциостатической кривой Pt ( СН3ОНадс) соответственно имеются две волны, первая отвечает окислению адсорбированного водорода, а вторая - хемосорбированного спирта. [11]
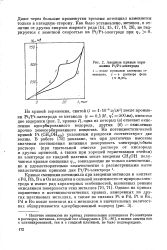 |
Анодные кривые заряжения Pt / Pt-электрода. [12] |
На кривой заряжения, снятой ( z 1 10 4 а / см2) после промывки Pt / Pt-электрода от метанола ( с 0 5Af, ср 500мв), имеются две задержки ( рис. 2, кривая 1), одна из которых ( а) отвечает окислению адсорбированного водорода, другая ( б) - окислению прочно хемосорбированного вещества. На потенциостатической кривой Pt ( СН3ОНадс) указанным процессам соответствуют две волны. [13]
Линейность кривой заряжения, по существу, означает постоянство емкости двойного слоя. Таким образом, при переходе от одной системы к другой k должна меняться пропорционально площади электрода J16 ], а отношение величин k для двух электродов дает отношение их удельных поверхностей. Приняв геометрическую и истинную поверхности жидкой ртути одинаковыми и, таким образом, установив k, Боуден и Ридил показали, что для твердых металлов истинная поверхность, как правило, значительно выше кажущейся, или геометрической, поверхности. [14]
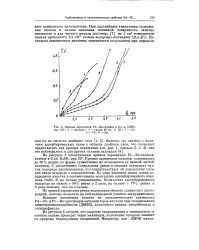 |
Кривые заряжения Pt-Re - сплавов в 0 1 н. H2SO4 при 20. 1 - платина. 2 - сплав 30 ат. % Re. 3 - 50. 4 - 10. 5 - Re. [15] |
Страницы: 1 2 3 4 5