Кривая - заряжение
Cтраница 4
В ходе измерения кривой заряжения палладиевого электрода наряду с процессом выхода растворенного водорода из решетки и его ионизации происходит снятие адсорбированного водорода. [46]
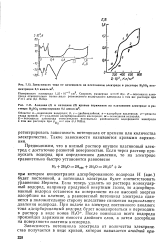 |
Зависимость тока от потенциала на платиновом электроде в растворе H2SO4 концентрации 0 5 кмоль / м3. [47] |
Такие зависимости называются кривыми заряжения. [48]
На рис. 4.15 представлена кривая заряжения для стали 06ХН28МДТ в промышленном перемешиваемом растворе гидр-оксиламинсульфата. Параллельно измеряли емкость двойного электрического слоя. Точки на кривой ABCZDEK соответствуют значениям потенциала в конце пауз между импульсами тока, точки на кривой MNOPS - значениям потенциала в моменты наложения катодного тока. После активации образца при ф - 0 7 В в течение 3 мин устанавливается потенциал ф - 0 32 В. Вначале потенциал медленно сдвигается в область положительных значений ( участок АВ), а через 1 - 1 5 ч происходит пассивация поверхности фст 0 23 В. Участок N0 свидетельствует о сдвиге потенциала от стационарного во времени. Сдвиг потенциала при поляризации достигает максимума ( ОР), затем поверхность активируется и цикл повторяется. [49]
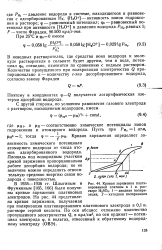 |
Кривая заряжения платинированной платины в 1 н. рас-гворе KkSO. / - анодная поляризация. 2 - катодная поляризация. [50] |
Площадь под водородным участком кривой заряжения пропорциональна работе десорбции водорода; по ее величине можно определить относительную среднюю энергию связи водорода с поверхностью. [51]
Каждый нижний пик на кривой заряжения связан с началом возникновения на поверхности электрода активного центра, а верхний пик соответствует началу его пассивации. [52]
Показано, что вид кривой заряжения определяется генезисом платиновой черни. [53]
Таким образом, из кривой заряжения вытекает логарифмическая изотерма адсорбции водорода на поверхности платинового электрода. [54]
Спол, полученной дифференцированием кривой заряжения в интервале 0 4 - 0 6 В, показывает их совпадение, что является результатом разделения областей адсорбции водорода и кислорода на платине при специфической адсорбции анионов. [55]
Таким образом, из кривой заряжения вытекает логарифмическая изотерма адсорбции водорода на поверхности платинового электрода. [56]
Такое объяснение участков обосновано сравнением кривой заряжения с кривыми адсорбции ионов в зависимости от потенциала электрода. [57]
Участок II называют двойнослойной областью кривой заряжения. [58]
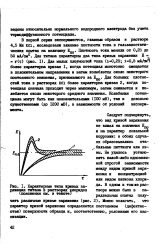 |
Характерные типы кривых заряжения титана в растворах хлоридов ( пояснения в тексте. [59] |
Следует подчеркнуть, что вид кривой заряжения не влиял на значения ЕПО и на характер локальной коррозии: в обоих случаях образовывались стабильные питтинги или язвы. [60]
Страницы: 1 2 3 4 5