Кривая - кристаллизация
Cтраница 3
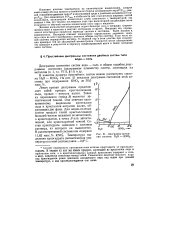 |
Диаграмма состоя-ния системы Н2О - KNOa. [31] |
Левая кривая диаграммы представляет собой кривую кристаллизации льда, правая - нитрата калия. Точка их пересечения ( точка Э) является эвтектической точкой. Она отвечает одновременному выделению кристаллов льда и кристаллов нитратов калия, образующих две фазы. Для водно-солевых систем продукт такой кристаллизации большей частью называют не эвтектикой, а криогидратом, а точку Э или эвтектической, или криогидратной точкой. Состав криогидрата одинаков с составом раствора, из которого он выделяется. [32]
Как видно из рис. 2, кривая кристаллизации имеет эвтектич. [34]
На рис. 35, а приведена кривая кристаллизации образца дициклопентила с чистотой 99 6 %, записанная самопишущим прибором с чувствительностью 0 016 град / мм. Для сравнения на рис. 35, б приведена кривая этого же образца дициклопентила той же чистоты, записанная самописцем с чувствительностью 0 07 град / мм. При сравнении рис. 35, а и б видно, что площадка кривой, записанной с большей чувствительностью, имеет наклон в несколько раз больший, чем у кривой, записанной менее чувствительным прибором. [35]
Если исходить из точки с, то кривая кристаллизации от этой точки пойдет по прямой до точки с, затем по пограничной кривой FD до эвтектической точки О. [36]
Для того чтобы проследить ход кристаллизации или кривую кристаллизации какого-либо расплава, например 6, состав которого находится внутри определенного поля устойчивости А-S - / - 1 - 2 ( рис. 131), через это поле проводят прямун линию, соединяющую составы Ь и S. [37]
В отличие от простейших двойных систем, где кривая кристаллизации состоит из двух ветвей, пересекающихся в эвтектической точке, на данной диаграмме имеется не две, а восемь ветвей и не одна, а четыре эвтектические точки В, D, F, И. Это обусловлено тем, что в зависимости от концентрации кислоты, H2SO4 и Н2О образуют гидраты различного состава. [38]
Из большинства опубликованных работ по определению чистоты органических соединений по кривым кристаллизации исследования Россини [2, 3] являются, по видимому, наиболее точными и наиболее теоретически обоснованными. [39]
Во всех разрезах кривые равновесия между жидкими фазами находятся под кривыми кристаллизации. [40]
Кривая 11, соответствующая давлению 0 5 ата, не пересекает кривую кристаллизации и поэтому кипение раствора происходит при любой концентрации. [41]
Но и для этого случая известен соответствующий метод расчета чистоты по кривым кристаллизации. [42]
В книге описан криоскопический метод определения чистоты органических и элементорганических веществ по кривым кристаллизации, записываемым автоматически на электронном пишущем потенциометре. [43]
Фазовая диаграмма простой эвтектической двухкомпонентной системы представлена на рис. 15.1. На этой диаграмме кривая XY представляет собой кривую кристаллизации вещества А в присутствии некоторого количества вещества В, а кривая ZY - кривую кристаллизации вещества В, к которому добавлено некоторое количество вещества А. В точке Y твердые А и В находятся в равновесии с массой расплава. В этой точке существуют одновременно три фазы, и система не имеет степеней свободы. Точка Y называется эвтектической точкой. [44]
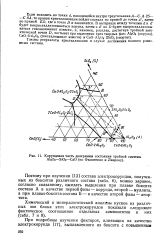 |
Корундовая часть диаграммы состояния тройной системы AUOs-SiOz-CaO ( по Филоненко и Лаврову. [45] |
Страницы: 1 2 3 4
