Кривая - фазовое равновесие
Cтраница 2
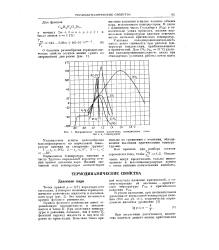 |
Пограничные кривые различных холодильных тов в s, ( - диаграмме. [16] |
Кривая фазового равновесия имеет ограниченную протяженность и заканчивается в точке К. При значениях температуры и давления, больших, чем в точке К, фазовый переход жидкости в пар или обратно не происходит. [17]
Кривые фазового равновесия, аналогичные изображенным на рис. 3, б (; тройной точкой на кривой равновесия пар-жидкость), рассматривались еще в [21 ] при обсуждении возможности рассматривать переход диэлектрик-металл как фазовый переход 1-го рода. [18]
Кривая фазового равновесия жидкой и газообразной фаз проходит всегда под острым углом к оси температур ( см. рис. 3.5), так как давление насыщенного пара возрастает с повышением температуры. Эта кривая имеет конечную протяженность и заканчивается в некоторой точке К, соответствующей определенным для данного вещества значениям температуры и давления. [19]
Кривая фазового равновесия между кристаллической и газообразной фазами в координатах р - Т проходит через начало координат; при Т - 0 давление пара над кристаллом равно нулю. [20]
 |
Зависимость между поверхностным натяжением и плотностью энергии когезии для растворителей. [21] |
Кривая фазового равновесия для систем с полимерным компонентом резко сдвинута в сторону низко-молекулярной жидкости. Такой сдвиг понятен, так как кинетическая подвижность тяжелых макромолекул очень мала. [22]
Кривая фазового равновесия практически представляет собою не одну линию, а систему кривых, отвечающих набору фракций полидисперсного полимера. Это касается преимущественно положения левой ветви кривой фазового равновесия, несколько в меньшей степени - области верхних критических точек и, по-видимому, в еще меньшей степени - правой части кривой, которая характеризует степень набухания полимера. Положение последней обусловлено по преимуществу энергией взаимодействия молекул низкомолекулярной жидкости с боковыми группами и звеньями полимерной цепи, а не кинетической подвижностью всей цепи. Кривые фазового равновесия для пары низкомолекулярных жидкостей ( Pi и Р2) и для системы растворитель ( Р) - полимер ( П) приведены на рис. 14, где заштрихованная область соответствует изменению положения кривых из-за полидисперсности полимера. [23]
 |
Схема ректификационной установки для разделения азеотропной смеси с минимумом температуры - кипения. [24] |
Кривая фазового равновесия 2 отвечает давлению р75 ата, под которым азеотропная точка имеет температуру кипения - 250 и состав: - 70 мол. [25]
 |
Фазовая диаграмма Вещества. [26] |
Кривая фазового равновесия жидкости и пара обрывается в критической точке / С Критическая точка соответствует определенным для данного вещества критическим значениям температуры Tv и давления рк. При больших значениях любого из этих параметров фазовый переход невозможен и невозможно указать однозначно фазовое состояние вещества. Так, при переходе из точки т в точку п по пути т - / - п невозможно указать, где именно произошел переход из жидкой фазы в газообразную. В этом проявляется условность подразделения состояния вещества на жидкое и газообразное, которые в сущности различаются лишь количественными характеристиками. Условно принимают, что жидкая фаза расположена выше кривой фазового равновесия и левее критической изотермы. Вся остальная область рассматривается как область газообразной фазы. [27]
Кривая фазового равновесия жидкости и пара, исходящая на диаграмме Г, Р из тройной точки, оканчивается в некоторой другой точке, носящей название критической. [28]
Кривая фазового равновесия жидкости и ее пара имеет конечную протяженность и заканчивается в некоторой точке К, соответствующей вполне определенным для данного вещества значениям температуры и давления ( фиг. [29]
 |
Фазовая диаграмма вещества. [30] |
Страницы: 1 2 3 4