Кривая - фазовое равновесие
Cтраница 3
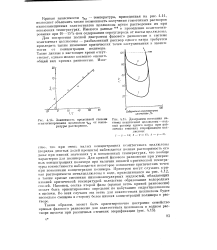
Кривая фазового равновесия жидкости и ее пара имеет на фазовой диаграмме конечную протяженность и заканчивается в критической точке / С. Критическая точка соответствует определенным для данного вещества критическим значениям температуры Тк и давления рк - При больших значениях любого из этих параметров фазовый переход невозможен и невозможно указать однозначно фазовое состояние вещества. Так, при переходе из точки m в точку п по пути m - / - п невозможно указать, где именно произошел переход из жидкой фазы в газообразную. В этом проявляется условность подразделения состояний вещества на жидкое и газообразное, которые в сущности различаются лишь количественными характеристиками. Условно принимают, что жидкая фаза расположена выше кривой фазового равновесия и левее критической изотермы. Вся остальная область рассматривается как область газообразной фазы. [31]
Кривая фазового равновесия жидкости и ее пара имеет конечную протяженность и заканчивается некоторой точкой К, соответствующей вполне определенным для данного вещества значениям температуры и давления. [32]
Кривая фазового равновесия АК заканчивается в точке К. Эта конечная точка фазового равновесия жидкость-пар называется критической точкой. [33]
Кривая фазового равновесия AD заканчивается в точке D. D является точкой прекращения существования двух фаз. [34]
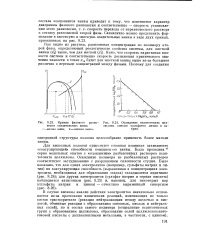 |
Осаждение ксантогената цел. [35] |
Кривые фазового равновесия осадительных ванн: 1 - мягкая ванна; 2-жесткая ванна. [36]
Кривой фазового равновесия называется линия на фазовой диаграмме, соответствующая состояниям равновесно сосуществующих фаз. [37]
Определена кривая фазового равновесия жидкость - пар для системы акролеин - акрилонитрил в интервале концентраций акролеина от 5 до 90 мол. Кроме того, установлено, что данная система имеет положительное отклонение от закона Рауля и с увеличением содержания акролеина в жидкой фазе от 5 до 90 мол. [38]
Определение кривой фазового равновесия по температурам, при которых происходит помутнение раствора полимера, в принципе является не вполне корректным. [39]
На кривой фазового равновесия давление ps и объем каждой фазы к ( 1), v №, а также энтальпии их z ( 1), i ( 2) и энтропии sO и s ( 2) являются функциями температуры. [40]
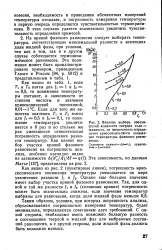 |
Влияние выбора соотношений количеств твердое тело - жидкость на погрешность определения криоскопическпго понижения температуры фазового равновесия. [41] |
На кривой фазового равновесия следует выбирать температуры, соответствующие максимальной разности в значениях доли жидкой фазы, при условии, что как в том, так и в другом случае соблюдается термодинамическое равновесие. [42]
Бимодальность кривых фазового равновесия может быть обусловлена влиянием окружения данного полимерного сегмента на его гибкость. Теоретически предполагается, что можно ожидать либо сжатия, либо расширения клубка полимера А в полимере В. Отсюда очевидно, что экспериментальное значение параметра ХАВ тесно взаимосвязано с микроструктурой смеси. Последние указывают на то, что в области составов смеси ( 20 - 40 % ПБМА), где наблюдается снижение ХАВ по сравнению с другими составами, происходит перераспределение поворотных изомеров в макромолекулах атактического ПС при введении в него ПБМА. Статистическая масса гране-изомеров увеличивается, что свидетельствует об изменении гибкости макромолекул. Очевидно, что в этих условиях макромолекулы ПС принимают в межфазном слое конформацию, обеспечивающую максимальное взаимодействие с макромолекулами ПБМА. Это и приводит к снижению параметра ХАВ и повышению термодинамической стабильности системы. [43]
Для кривой фазового равновесия при умеренных концентрациях полимера при наличии нижней критической температуры совместимости наблюдается некоторое понижение критических точек при повышении концентрации полимера. Примером могут служить кривая растворимости метилцеллюлозы в воде, приводившаяся на рис. 4.12, а также кривые смешения низкомолекулярных жидкостей, обладающих нижней критической температурой вследствие образования водородных связей. Наконец, состав второй фазы ( правая ветвь кривой равновесия) может быть ориентировочно определен по набуханию гидратцеллюлозы в щелочи. Во всех случаях эта ветвь для ксаптогената целлюлозы будет несколько смещена в сторону более низких концентраций полимера в растворе. [45]
Страницы: 1 2 3 4