Потенциальная кривая
Cтраница 2
Потенциальные кривые для чистых компонентов А и В при поддержании того же потенциала, что и на сплаве, сместятся вниз, но не совпадут своими минимумами с минимумами потенциальных кривых составляющих А и В. Из-за увеличения наклона потенциальной кривой в связи с торможениями при ионизации компонента А из сплава и снижения его свободной энергии энергия активации реакции растворения из сплава возрастает и анодный процесс тормозится. [16]
Потенциальные кривые для атомов достигают соответствующих предельных значений ( на обоих рисунках, обозначенных пунктирными прямыми для Na - j - C1 и Н -) - Н) гораздо быстрее. Электростатическое притяжение, следовательно, действует на значительно больших расстояниях, чем силы гомеополярной связи. Характерно, далее, что расстояние между предельными значениями для кривых I и / / на рис. 64 и 65 сильно различаются. Это расстояние, представляющее собой разницу днереий между состоянием из свободных ионов А - f - B - и состоянием из свободных атомов А 4 В в первом случае равно 1 39, во втором 12 88 эв. Его можно выразить через разность / А-ЕВ, где JA - работа ионизации атома А и Es - сродство к электрону атома В. А - ЕЪ велико, то образование молекулы происходит из атомов. [17]
Потенциальные кривые для атомов достигают соответствующих предельных значений ( на обоих рисунках, обозначенных пунктирными прямыми для Na - j - C1 и Н - - Н) гораздо быстрее. Электростатическое притяжение, следовательно, действует на значительно больших расстояниях, чем силы гомеополярной связи, Характерно, далее, что расстояние между предельными значениями для кривых / и / / на рис. 64 и 65 сильно различаются. Это расстояние, представляющее собой разницу энергий между состоянием иа свободных ионов А -) - В - и состоянием из свободных атомов А - 4 - В в первом случае равно 1 39, во втором 12 88 ее. [18]
Потенциальные кривые для чистых компонентов А и В при установлении на последних того же потенциала, что и на интер металлической фазе, сместятся вниз, но они не совпадут своими минимумами с минимумами потенциальных кривых составляющих А и В. [19]
Потенциальные кривые для ионов сравнительно медленно-стремятся к нулевому значению - действие электростатического притяжения простирается на гораздо большие расстояния, чем действие ковалентной связи. [20]
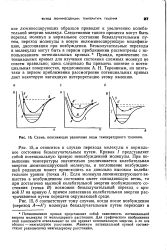 |
Схема, поясняющая различные виды температурного тушения. [21] |
Потенциальная кривая представляет собой зависимость потенциальной энергии молекулы от межъядерного расстояния. Для графического изображения этой зависимости откладывают по оси ординат потенциальную энергию, а по оси абсцисс - межъядерное расстояние. Минимум потенциальной кривой соответствует равновесному межъядерному расстоянию. [22]
Потенциальная кривая может быть в принципе построена путем квантомеха-нического расчета, однако последний в настоящее время осуществим лишь для простейших случаев, и обычно пользуются эмпирическими данными, полученными из колебательно-ротационных спектров. [23]
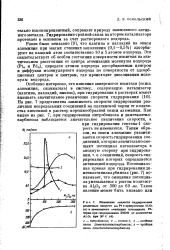 |
Изменение скорости видрирования различных веществ на Pt в присутствии АЬОз ( а и зависимость смещения потенциала Pt-черни при гидрировании ДМЭК от количества А1 03 при 20 С ( б. [24] |
Потенциальная кривая при гидрированииди-метилэтинилкарбинола ( рис. 7) показывает, что смещение потенциала уменьшается с ростом количества А1203 от 300 до 60 мв. [25]
Потенциальные кривые для молекулы N0 и молекулярных ионов N0 - и NO, полученные на основе спектроскопических и других экспериментальных данных. [26]
Потенциальные кривые иода изображены на рис. XXIX. Отсчеты идут от нулевой колебательной энергии, и энергию диссоциации получают при О К. [27]
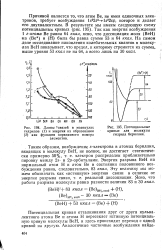 |
Длины связей в молекулах. [28] |
Потенциальная кривая отталкивания друг от друга нульва-лентного атома Be и атома Н пересекает истинную потенциальную кривую молекулы ВеН, и здесь происходит переход с одной кривой на другую. [29]
Подобная потенциальная кривая наблюдается, если действуют только кулоновские силы взаимодействия или электрические силы отталкивания преобладают над силами адгезии. [30]
Страницы: 1 2 3 4 5