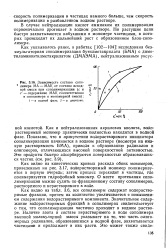
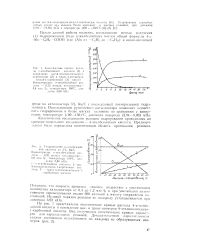
Кинетическая кривая - расход
Cтраница 1
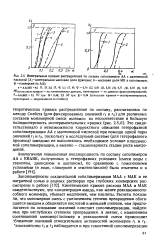 |
Интегральные кривые распределения по составу сополимеров АА с малеиновои кислотой ( Х - интегральная массовая доля фракции. а-массовая доля МК в сополимере. ф - конверсия по А А. [1] |
Кинетические кривые расхода МАА и МАК свидетельствуют, что концентрация амида, как менее реакционноспо-собного мономера, убывает медленнее, чем кислоты. Расчеты показали, что мономерная смесь с увеличением степени превращения обогащается амидом и обедняется кислотой в меньшей степени, чем предполагается на основании значений констант сополимеризации, найденных при неглубоких степенях превращения. [2]
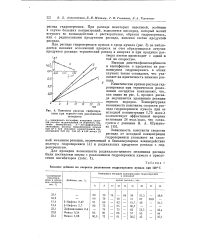 |
Кинетика расхода гидроперекиси при термическом разложении оксидатов. [3] |
Кинетические кривые расхода гидроперекиси при термическом разложении оксидатов показывают, что, как видно из рис. 4, процесс распада подчиняется уравнению реакции первого порядрса. [4]
Как видно из кинетических кривых расхода обоих мономеров, приведенных на рис. 3.17, водорастворимый мономер полимеризу-ется в первую очередь; затем процесс переходит в частицы, где полимеризуется гидрофобный мономер. [6]
На основе анализа кинетических кривых расхода кетона показано, что в любой момент времени кетон находится в равновесии ( Т) с полупер-оксикеталем. [7]
На рис. 1 представлены кинетические кривые расхода 4-этило еи-зойной кислоты и накопление цис - и транс-изомеров 4-этилциклогсксап - 1-карбоновой кислоты. Вид полученных кинетических кривых характерен для параллельных реакций. [9]
На рис. 1 представлены кинетические кривые расхода л-цимола во времени н накопления продуктов окисления. [10]
На рис. 1 представлены кинетические кривые расхода я-цимола во времени и накопления продуктов окисления. Из полученных данных видно, что основным продуктом окисления является п - ИПБК. [11]
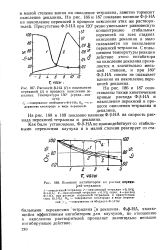 |
Влияние ингибиторов на распад переки - [ сей тетралина. [12] |
На рис. 186 и 187 сопоставлены также кинетические кривые расхода Ф - - НА и накопления перекисей в процессе окисления тетралина и декалина. [13]
Из данных рис. 3, на котором приведены кинетические кривые расхода ГПК при различном содержании воды в исходной смеси, следует, что скорость реакции замедляется с увеличением содержания воды в смеси. [14]
Во время перехода от большей оптической плотности раствора к меньшей раствор не титруется. В это время регистрируется обычная кинетическая кривая расхода ДНХФ и по изменению оптической плотности реакционной смеси от времени можно определять начальную скорость реакции при данной концентрации субстрата. [15]
Страницы: 1 2