Реальная поляризационная кривая
Cтраница 2
Поляризационная диаграмма коррозии, построенная на основании реальных и идеальных поляризационных кривых, представлена на рис. 22, где: 1 и 2 - реальные поляризационные кривые; 3 и 4 - идеальные поляризационные кривые. [16]
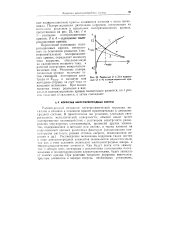 |
Реальные ( 1 и 2 и идеальные ( 3 и 4 поляризационные кривые. [17] |
Поляризационная диаграмма коррозии, построенная на основании реальных и идеальных поляризационных кривых, представлена на рис. 22, где: / и 2 - реальные поляризационные кривые; 3 и 4 -идеальные поляризационные кривые. [18]
Реальные поляризационные кривые ( см. рис. 9) начинают свой ход от стационарного значения электродного потенциала металла Уст в данной среде и фактически являются продолжением идеальных поляризационных кривых, которые берут начало от обратимых электродных потенциалов анодной и катодной реакции данного коррозионного элемента ( V A и V K) - Реальные поляризационные кривые ( катодные и анодные) наносят на коррозионную диаграмму и по их форме и взаимному расположению судят не только о максимально возможной величине коррозионного тока в данных условиях, но и о возможности торможения коррозионного процесса. Таким путем выявляется тот этап коррозионного процесса, который протекает с наибольшим затруднением и контролирует скорость разрушения металла в данной среде. Все защитные мероприятия направлены на то, чтобы усилить тормозящее действие контролирующего фактора. [19]
Возможность практического использования полученного соотношения для определения деформационного изменения тока коррозии обосновывается так же, как и в известном методе снятия реальных поляризационных кривых для определения скорости коррозии металла на основе кинетической теории коррозии: идеальные поляризационные кривые, определяющие стационарный потенциал и ток коррозии, рассматриваются как продолжение тафелевских участков реальных поляризационных кривых. Это, очевидно, справедливо для электрохимически гомогенной поверхности, но также может быть принято для технических металлов ( железа, никеля, свинца и Др. На рис. 59 реальные поляризационные кривые показаны сплошными линиями. Для практического расчета скорости коррозии в формулу ( 232) следует подставлять величины сдвигов потенциалов, определенные сечением реальных анодных и катодных поляризационных кривых для произвольно выбранного значения плотности тока гальваностатической поляризации в пределах тафелевских участков. Из соотношения ( 229) видно, что изменение стационарного Потенциала вследствие деформации электрода не является однозначной функцией термодинамического состояния металла ( обу-словливающего анодное поведение) из-за участия катодного про-щесса. [20]
Возможность практического использования полученного соотношения для определения деформационного изменения тока коррозии обосновывается так же, как и в известном методе снятия реальных поляризационных кривых для определения скорости коррозии металла на основе кинетической теории коррозии: идеальные поляризационные кривые, определяющие стационарный потенциал и ток коррозии, рассматриваются как продолжение тафелевских участков реальных поляризационных кривых. На рис. 66 реальные поляризационные кривые показаны сплошными линиями. Для практического расчета скорости коррозии в формулу ( 245) следует подставлять величины сдвигов потенциалов, определенные сечением реальных анодных и катодных поляризационных кривых для произвольно выбранного значения плотности тока гальваностатической поляризации в пределах тафелевских участков. [21]
Пересечение идеальных поляризационных кривых, построенных на основании реальных ( экспериментальных) поляризационных кривых, определяет величину тока коррозии, обусловленную не наложением внешнего тока, а работой внутренних микрогальванических пар. Реальные поляризационные кривые получают путем смещения потенциала электрода от ЕКОрр в анодную или катодную сторону за счет тока от внешнего источника. При малых внешних токах реальные и идеальные поляризационные кривые значительно разнятся, но с ростом тока они сближаются, а затем совпадают. [22]
 |
Реальные ( 1 и 2 и идеальные ( 3 и 4 поляризационные кривые. [23] |
Пересечение идеальных поляризационных кривых, построенных на основании реальных ( экспериментальных) поляризационных кривых, определяет величину тока коррозии, обусловленную не наложением внешнего тока, а работой внутренних микрогальванических пар. Реальные поляризационные кривые получают путем смещения потенциала электрода от Епорр в анодную или катодную сторону за счет тока от внешнего источника. При малых внешних токах реальные и идеальные поляризационные кривые значительно разнятся, но с ростом тока они сближаются, а затем совпадают. [24]
Возможность практического использования полученного соотношения для определения деформационного изменения тока коррозии обосновывается так же, как и в известном методе снятия реальных поляризационных кривых для определения скорости коррозии металла на основе кинетической теории коррозии: идеальные поляризационные кривые, определяющие стационарный потенциал и ток коррозии, рассматриваются как продолжение тафелевских участков реальных поляризационных кривых. На рис. 66 реальные поляризационные кривые показаны сплошными линиями. Для практического расчета скорости коррозии в формулу ( 245) следует подставлять величины сдвигов потенциалов, определенные сечением реальных анодных и катодных поляризационных кривых для произвольно выбранного значения плотности тока гальваностатической поляризации в пределах тафелевских участков. [25]
Тафелевские участки поляризационных кривых соответственно располагаются следующим образом ( рис. 59, сплошные линии): анодный сдвигается в сторону отрицательных значений потенциала на величину, несколько меньшую, чем Аф, катодный - в сторону положительных значений потенциала. Именно такой характер влияния деформации на реальные поляризационные кривые выявлен экспериментально [60, 2] ( см. гл. [26]
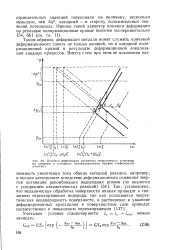 |
Влияние деформации активного гетерогенного электрода на анодную и катодную поляризационные кривые ( тафелевские участки. [27] |
Аф, катодный - в сторону положительных значений потенциала. Именно такой характер влияния деформации на реальные поляризационные кривые выявлен экспериментально [54, 66] ( см. гл. [28]
Решение практических задач гальванотехники и электрохимической защиты металлов от коррозии требует исследования электрического поля электродов с учетом их поляризации. Для случая линейной зависимости между потенциалом электрода и плотностью тока Ю. Я. Иосселем предложен способ моделирования с помощью непроводящих перфорированных покрытий 11L Однако реальные поляризационные кривые не являются линейными, поэтому рассмотрение нелинейной задачи представляет несомненный интерес. [29]
Возможность практического использования полученного соотношения для определения деформационного изменения тока коррозии обосновывается так же, как и в известном методе снятия реальных поляризационных кривых для определения скорости коррозии металла на основе кинетической теории коррозии: идеальные поляризационные кривые, определяющие стационарный потенциал и ток коррозии, рассматриваются как продолжение тафелевских участков реальных поляризационных кривых. Это, очевидно, справедливо для электрохимически гомогенной поверхности, но также может быть принято для технических металлов ( железа, никеля, свинца и Др. На рис. 59 реальные поляризационные кривые показаны сплошными линиями. Для практического расчета скорости коррозии в формулу ( 232) следует подставлять величины сдвигов потенциалов, определенные сечением реальных анодных и катодных поляризационных кривых для произвольно выбранного значения плотности тока гальваностатической поляризации в пределах тафелевских участков. Из соотношения ( 229) видно, что изменение стационарного Потенциала вследствие деформации электрода не является однозначной функцией термодинамического состояния металла ( обу-словливающего анодное поведение) из-за участия катодного про-щесса. [30]
Страницы: 1 2 3