Кондуктометрическая кривая
Cтраница 4
 |
Кондуктометрические кривые титрования солей слабых оснований раствором NaOH ( кривые а, б, в, з, к, л и солей слабых кислот раствором НС1 ( кривые г, д, е, ж, и, м. [46] |
С уменьшением степени гидролиза соли формы кондуктометрических кривых изменяются. [47]
Нейтрализация кислот в более разбавленных растворах приводит к закруглению кондуктометрической кривой вблизи точки эквивалентности. [48]
Следует учитывать, что графическое установление точек эквивалентности на кондуктометрических кривых позволяет использовать в какой-то мере обратимые химические реакци-и, что представляет существенное преимущество кондуктометрического метода титрования. [49]
Соли кислот, имеющих рКа 4 - 9, дают кондуктометрические кривые с. [50]
Реакция нейтрализации кислоты до Na3PO4 сильно обратима, и излом кондуктометрической кривой, фиксирующий полную нейтрализацию кислоты, не обнаруживается. Поэтому кондуктометрическое определение фосфорной кислоты основывается на нейтрализации первого кислотного эквивалента. [51]
 |
Ковдуктометрические кривые титрования при использовании реакции осаждения, окисления - восстановления и комплексообразования. [52] |
При кондуктометрическом титровании необходимо, прежде всего, чтобы излом кондуктометрической кривой позволял устанавливать точку эквивалентности с достаточной точностью. [53]
Можно привести много других примеров нелинейного изменения электропроводности раствора на ветвях кондуктометрических кривых, вызываемого смещением ионных равновесий, что детально рассмотрено в последующих главах. При этом следует, учитывать, что если реакция протекает количественно, несмотря на нелинейное изменение электропроводности раствора излом кривой в точке эквивалентности резко выражен. Очень часто нелинейное изменение электропроводности раствора наблюдается только в начале процесса титрования или на первой половине кондуктометрической кривой до точки эквивалентности. В некоторых случаях обнаруживаются минимумы или максимумы на кривых титрования до точки эквивалентности, не имеющие аналитического значения. [54]
Это становится особенно заметным вблизи точки эквивалентности и выражается в плавности изгиба кондуктометрической кривой, поскольку в начале титрования обратимость реакции подавляется, так как в растворе находится избыток определяемого вещества, а в конце титрования это же влияние оказывает избыток титранта. [55]
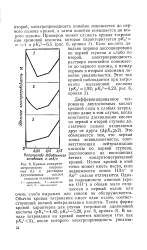 |
Кривые кондукто-метрического титрования 0 1 н. растворов двухосновных кислот сильным основанием. [56] |
Количества Ыабя ентгв Расположена на восходящих основания, г-экб / я ветвях кондуктометрической кривой. Излом кривой в этой точке может иметь место, если подвижности ионов НАп - и Ап2 - сильно отличаются. [57]
Образующиеся в растворе СНзСОО - - ионы также подавляют диссоциацию СН3СООН, поэтому кондуктометрическая кривая изогнута. Однако в связи с увеличением степени диссоциации СНзСООН в разбавленных растворах не происходит полного подавления ее диссоциации под влиянием СНзСОО - - ионов. Равновесная концентрация водородных ионов в этих условиях остается достаточно высокой, и при их нейтрализации электропроводность понижается. [58]
Страницы: 1 2 3 4