Равновесная кривая
Cтраница 2
Обычно равновесная кривая АВ не описывается прямой линией; последней по причинам, обсужденным выше, является рабочая линия. [16]
Равновесная кривая чувствительного элемента является одной из основных характеристик качества работы регулятора. Форма равновесной кривой существенно влияет на форму регуляторной характеристики двигателя. [17]
Равновесные кривые все-режимного механического регулятора с переменной предварительной затяжкой Df p пружин. [18]
Равновесную кривую строят на основе рав-четов, используя соответствующие законы равновесия фаз, или по опытным данным. [19]
Равновесную кривую строят по табличным данным, имеющимся в справочниках и монографиях. [20]
Если равновесная кривая отклоняется от прямолинейного вида, го ее разбивают на несколько участков и ведут расчет по участкам, - принимая каждый из них за прямолинейный. [21]
Поскольку равновесные кривые для компонентов сырого бензола сравнительно близки к прямым линиям, а рабочая линия при типичных процессах абсорбционного выделения сырого бензола изображается прямой, можно применять упрощенные расчетные уравнения, например уравнение (1.8), основанное на KQa, уравнение (1.14), основанное на концепции единичной ступени массообмена, и уравнение (1.15), основанное на концепции теоретической тарелки. Как и при параметре LMJmGM, значение LklG, равное единице, выражает минимальное отношение жидкости к газу, которое может обеспечить полное удаление нежелательного компонента в колонне бесконечной высоты. Для практических случаев цитируемые исследователи указывают значения L & / G, равные около 1 3, как типичные для абсорбции сырого бензола. [22]
 |
Коэффициенты сжимаемости углеводородов в зависимости от приведенного давления и приведенной температуры.| Коэффициенты активности углеводородов с числом атомов более трех. [23] |
Такие равновесные кривые требуются для расчета ректификации при тонком разделении отдельных фракций с целью получения чистых компонентов. [24]
Рассмотрим равновесные кривые температура кипения - состав смеси ( рис. 7 6 и в, стр. Эти графики имеют два вида: с минимумом температуры кипения и с максимумом, в которых кривые состава пара и жидкости касаются друг друга. Точка максимума или минимума температуры кипения делит весь график на две половины, из которых каждая подобна кривым на рис. 7, а, и к ней могут быть отнесены все те же рассуждения. Из графика с минимумом температуры кипения следует, что, какой бы исходный состав жидкости мы ни взяли, мы будем в процессе фракционирования получать жидкость того состава, который срответствует минимуму температуры кипения, а в остатке будет чистая жидкость А или В, в зависимости от того, исходили ли мы из состава, соответствующего левой или правой от минимума части кривой. В случае кривой с максимумом температуры кипения картина сходная, только отгон по мере фракционирования будет обогащаться чистой жидкостью А или В, в зависимости от того, соответствовал ли исходный состав левой или правой части кривой ( считая от максимума); останется жидкость, все более приближающаяся к составу, соответствующему максимуму температуры кипения. Составы жидкостей, соответствующие минимуму и максимуму кривой, называются постоянно кипящими или азеотропными смесями. Они не разделимы фракционной перегонкой. [25]
Определение равновесной кривой по условию равных площадей называется правилом Максвелла. [26]
Знание равновесных кривых всех элементов дает возможность построить равновесную кривую системы автоматического регулирования двигателя. [27]
Из равновесных кривых этих реакций для железа и хрома ( фиг. А) при температуре 1100 С можег быть допущено в 1000 раз большее содержание влаги, чем для восстановления хрома. С повышением температуры требования к осушке снижаются. Поэтому активные металлы ( см. табл. 3) сваривают при более глубокой осушке и более высокой температуре. [28]
 |
Влияние азота на гидратообразование сжиженных газов. [29] |
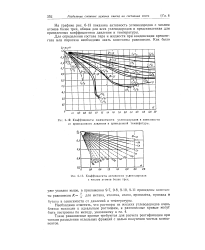
Сравнение полученных равновесных кривых показывает, что при одинаковой температуре для образования гидратов в системе I требуется большее давление, чем в системе И, или, наоборот, при одинаковом давлении для образования гидратов в системе I необходима более низкая температура, чем в системе II, и эта разница тем больше, чем больше давление азота. Из рис. 2 также видно, что в системе I гидратообразование происходит только до температуры 5 5 С. [30]
Страницы: 1 2 3 4 5