Кристалл - белок
Cтраница 2
Многими авторами убедительно показано, что кристаллы белка синтезируются из аминокислот, поступающих из питательной среды и из цитоплазмы вегетативной клетки. Кристаллы имеют кубическую или тетрагональную форму. [16]
Положим, мы ищем амплитудный ко - ячейка кристалла белка. [17]
При рентгеноструктурном анализе белка неизвестной структуры регистрируется интерференционная картина от кристалла белка. [18]
Как оказалось, ферменты, приготовленные по Нортропу, являются прекрасно выраженными кристаллами белка, не оставляющими сомнения в их однородности. Впрочем, эти кристаллические ферменты мало похожи на обычные кристаллы минеральных веществ или органических соединений; они содержат значительное количество воды и солей и могут существовать только в насыщенном маточном растворе. При попытках высушивания они разрушаются. [19]
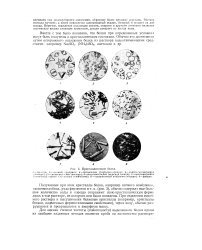 |
Кристаллические белки. [20] |
При отделении маточного раствора и высушивании белковые кристаллы ( например, кристаллы белков, наделенных ферментативными свойствами), теряя воду, обычно разрушаются и превращаются в аморфную массу. [21]
Современный уровень знания деталей конформации белков основан почти исключительно на результатах исследования кристаллов белков методом дифракции рентгеновских лучей. [22]
Вескими доказательствами белковой природы фермента являются его получение в чистом виде и выделение в форме кристаллов белка. К настоящему времени получено более 1000 кристаллических ферментов. [23]
Поскольку определение электронных плотностей с небольшим разрешением ( 0 5 нм) не столь трудоемко, обычно начинают исследование структуры кристалла белка с этого этапа. Развитие этого метода, осуществленное в 1952 - 1960 гг. лабораториями Кендрью и Перутца, стало значительным научным достижением. К настоящему времени известны пространственные структуры более 50 белков. [24]
Сущность этого метода заключается во введении в строго определенные участки полипептидной цепи белка атомов тяжелых металлов ( например, атомов ртути) и сравнении рентгенограмм кристаллов свободного белка и изоморфных замещенных структур. Расшифровка получаемых карт электронной плотности позволяет создать трехмерную картину молекулы белка. [25]
В этом сообщении очень кратко рассмотрена история представлений и исследований, касающихся воды, обсуждены необычные свойства парциальной молярной сжимаемости гидрофобных веществ в воде и изложены основные результаты исследований локализации молекул воды в кристаллах белков методами рентгеновской и нейтронной спектроскопии. [26]
Методы охлаждения водных р-ров, испарения р-рителя и температурного перепада используют для выращивания кристаллов сегнетовой соли размером 30 - 80 см и КН2РО4 размером 30 - 60 см, применяемых для пьезоэлементов; методом высаливания выращивают кристаллы белков и нуклеиновых к-т; методом хим. кристаллизации-микрокристаллы А § 1 размером 0 1 - 10 мкм для фотоэмульсий; методом гидротермального синтеза-кристаллы кварца н сапфира размером до 50 см для приборостроения н ювелирной пром-сти; методом охлаждения р-ра в расплаве металла-кристаллы ОаР размером до 1 см для электролюминесцентных датчиков; охлаждения р-ра в расплаве солей - - иттрий-алюминиевого граната У3А15О12 размером до 2 см для твердотельных лазеров. [27]
Молекулы белков могут быть выделены и кристаллизованы. Кристаллы белков, несмотря на то, что их молекулы содержат тысячи атомов, удается изучить методами рентгеноструктурного анализа и установить их структуру. Задача эта исключительно сложна, и не удивительно, что к настоящему времени известна структура лишь шести белков. [28]
Кристаллы белков легко разбухают и теряют свою форму. Кристаллы белков найдены в клетках некоторых растений. [29]
В кристаллическом виде получены только глобулярные белки; фибрилярные белки неспособны кристаллизоваться. Кристаллы белков, растущие из растворов, содержат растворитель, который входит в структуру белка, так что удаление его вызывает потерю кристалличности. [30]
Страницы: 1 2 3 4