Кристаллизация - твердая фаза
Cтраница 2
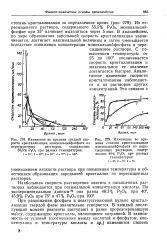 |
Изменение во времени средней ско - [ IMAGE ] Изменение во вре. [16] |
При разложении фосфата в незагустевающей пульпе кристаллизация твердой фазы значительно ускоряется. В каждый последующий момент реагенты поступают в ранее прореагировавшую массу, содержащую кристаллы, являющиеся затравкой. [17]
 |
Схжа каскада для противоточной кристаллизации из раствора. [18] |
Другими вариантами фракционированной кристаллизации являются метод последовательной кристаллизации твердой фазы с возвратом в цикл маточных растворов и метод многократной кристаллизации маточного раствора с возвратом в цикл твердой фазы. Если примесь концентрируется в жидкой фазе, то следует использовать первый из указанных методов. Если же примесь концентрируется в твердой фазе, то целесообразнее применять второй метод. Существенное преимущество этих методов перед методом дробной кристаллизации заключается в том, что при их осуществлении может быть использован принцип противотока, обусловливающий большую производительность. [19]
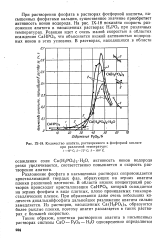 |
Количество апатита, растворенного в фосфорной кислоте. [20] |
Разложение фосфата в насыщенных растворах сопровождается кристаллизацией твердых фаз, образующих на зернах апатита пленки различной плотности. В области низких концентраций растворов происходит кристаллизация СаНРС4, который осаждается на зернах фосфата в виде плотных, плохо проницаемых тонкокристаллических пленок. При образовании даже очень небольших количеств дикальциифосфата дальнейшее разложение апатита сильно замедляется. Из растворов, насыщенных Са ( Н2РО4) 2, образуются более рыхлые пленки, поэтому апатит разлагается в таких растворах с большей скоростью. [21]
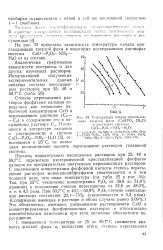 |
Температура начала кристаллизации твердой фазы ( СаНРО4 2Н2О. [22] |
На рис. 33 приведена зависимость температуры начала кристаллизации твердой фазы в некоторых исследованных растворах системы СаО - Р2О5 - МН3 - Н2О от их состава. [23]
Приводятся результаты исследования вещественного состава и условий кристаллизации твердых фаз в системе. MgO - MgClz - HSO; рассматриваются закономерности развития кристаллизационных дисперсных структур твердения в процессе химического превращения дисперсной фазы концентрированных суспензии при изменении уровня пересыщения среды, дисперсности и природы исходной твердой фазы и новообразований. [24]
Приводятся результаты исследования вещественного состава и условий кристаллизации твердых фаз в системе MgO - MgClz - Н О; рассматриваются закономерности развития кристаллизационных дисперсных структур твердения в процессе химического превращения дисперсной фазы концентрированных суспензий при изменении уровня пересыщения среды, дисперсности и природы исходной твердой фазы и новообразований. [25]
Приводятся результаты исследования вещественного состава и условий кристаллизации твердых фаз в системе. MgO - MgClj - Н2О; рассматриваются закономерности развития кристаллизационных дисперсных структур твердения в процессе химического превращения дисперсной фазы концентрированных суспензий при изменении уровня пересыщения среды, дисперсности и природы исходной твердой фазы и новообразований. [26]
Еще одна причина неподвижности якоря может заключаться в кристаллизации твердой фазы из состава рабочей среды в зазоре между поверхностями трения. Как правило, это происходит в тех случаях, когда процесс кристаллизации происходит при длительном неподвижном нахождении якоря в одном из крайних положений. В числе причин, вызывающих потерю подвижности якоря, может быть сосредоточение в зазоре пары трения большого количества продуктов износа. [27]
Концентрации компонентов системы ( а также соответствующие области кристаллизации твердых фаз) представляются здесь суммарно, по меньшей мере, по два компонента совместно. [28]
В данном случае оптимальная проекция допускает обзор областей кристаллизации твердых фаз, включающих какие-либо два компонента пятерной системы. [29]
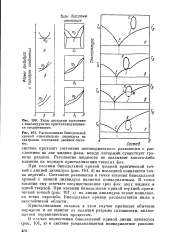 |
Типы диаграмм состояния с инконгруэнтно кристаллизующимися соединениями.| Расположение бинодальной кривой относительно ликвидуса на диаграмме состояния двойной системы. [30] |
Страницы: 1 2 3 4