Кристаллизация - твердая фаза
Cтраница 4
В случае тройной системы с эвтектикой на фазовой диаграмме имеются пов-сти кристаллизации отдельных твердых фаз, линии, отвечающие совместной кристаллизации двух твердых фаз, и ионвариантная точка, отвечающая равновесию расплава с тремя твердыми фазами. Диаграмма плавкости тройной системы описывает т-ру плавления смесей разл. На практике, однако, используют проекции изотермич. [46]
Как было показано Хлопиным [42], численное значение Я зависит от скорости кристаллизации твердой фазы. Если в процессе образования осадка в любой момент времени имеет место истинное равновесие между поверхностным слоем растущих кристаллов и рас - твором ( рост кристаллов идет достаточно медленно), то коэффициент кристаллизации Я примет свое максимальное значение, численно равное D. Коэффициент кристаллизации Я, в этом случае также является физико-химической константой, полностью характеризующей данную систему. [47]
При 100 С К80 %, что является предельной величиной для условий кристаллизации твердой фазы, образующей проницаемые пленки из монофосфатов кальция. Очевидно достижению равновесия препятствует уменьшение скорости процесса разложения под влиянием различных факторов, в частности, при увеличении степени нейтрализации жидкой фазы и снижении температуры. [48]
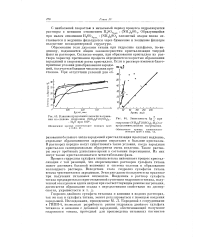 |
Влияние продолжительности нагревания на степень гидролиза ( NH TiC SO Н20 при 100.| Зависимость lg - при. [49] |
Образование геля двуокиси титана при гидролизе сульфатов, по-видимому, подчиняется общим закономерностям кристаллизации твердой фазы из растворов. Согласно теории, при образовании кристаллов из раствора характер протекания процесса определяется скоростью образования зародышей и скоростью роста кристаллов. Если в растворе имеются благоприятные условия для образования зароды - а шей, получается большое число мелких кри-сталлов. [50]
 |
Принципы построения изотермических диаграмм растворимости первого типа для трех - и четырехкомпонентных систем. [51] |
Конечное значение на этих диаграммах имеют лишь линии упаривания раствора, а также линии кристаллизации твердых фаз, представленных гидратами. Следовательно, применение правила рычага для графического расчета процессов кристаллизации ( как политермической, так и изотермической) или растворения при построении диаграмм второго типа невозможно в тех случаях, когда кристаллизуются ( или растворяются) безводные соединения. [52]
Как было показано [43], химическое созревание протекает также в стадии первого созревания параллельно процессу кристаллизации твердой фазы эмульсии. [53]
Таким образом, имеется ряд экспериментальных данных, которые противоречат представлению об образовании фазовых контактов путем кристаллизации твердой фазы из поверхностного раствора и нет ни одного факта, который доказывал бы, что слеживаемость протекает в соответствии с кристаллизационным механизмом. [54]
На рис. 88 дано изображение р - / - проекции систем такого рода, в которых кристаллизация твердых фаз не происходит и в которых критические кривые не обрываются в точках Р и Q. Но в тех случаях, когда происходит кристаллизация и критические кривые обрываются в точках Р и Q, область расслаивания ( сосуществования двух жидкостей и газа - жх ж2 газ) и примыкающие к этой области участки критических кривых становятся метастабильными. [55]
Графическое изображение и расчет процесса кристаллизации при охлаждении упрощается, когда заданы температуры начала и конца кристаллизации твердой фазы. [56]
Для получения прозрачной суперфосфорной кислоты следует упаривать кислоту со скоростью, обеспечивающей температуру процесса ниже температуры кристаллизации твердой фазы. [57]
Графическое изображение и расчет процесса кристаллизации при охлаждении значительно упрощаются, когда заранее заданы температуры начала и конца кристаллизации твердой фазы. В этом случае на треугольную диаграмму растворимости наносятся две изотермы, соответствующие указанным температурам. [58]
Разложение фосфата в фосфорной кислоте происходит в насыщенных растворах солей моно - и дикальцийфосфата, одновременно оно сопровождается кристаллизацией твердых фаз. На частицах сырья образуются пленки различной проницаемости. [59]
Практическая же возможность завершения процесса в соответствии с теоретическим состоянием равновесия зависит от скорости разложения фосфата и от условий кристаллизации твердых фаз. [60]
Страницы: 1 2 3 4