Лектрон
Cтраница 3
С электронной точки зрения окислением называется процесс, ри котором происходит потеря электронов, а восстановлением - роцесс, связанный с присоединением электронов. Вещества, ко-эрые при окислительно-восстановительных реакциях теряют лектроны, называются восстановителями, а вещества, присоеди-яющие электроны-окислителями. Следовательно, восстановись при реакции всегда окисляется, а окислитель-восстанавли-ается. [31]
Эллиптическая чески изменяется не только угол о орбита лектрона в атоме длта радиус. [32]
Суммарная реакция показывает, что равновесие окисления - восстановления определяется активностью ионов водорода. Платина, опущенная в насыщенный раствор хингидрона, являясь передатчиком лектронов между хиноном и гидрохиноном, приобретает потенциал, величина которого зависит от активности ( концентрации) ионов водорода. [33]
Они определяются вумя режимами токораспределения. При 0f / c 0 75С / а устанавливается режим прямого перехвата лектронов сеткой. В этом режиме на управляющую сет -: у попадает сравнительно небольшое количество элек-ронов. Электроны, пролетев-иие между прутками сетки, несмотря на некоторое ис-фивление траекторий, вызванное притяжением элек-ронов к положительно заряженным пруткам, достигают шода. [34]
Во ПА группу периодической системы Д. И. Менделеева входят элементы Be, Mg, Ca, Sr, Ba и Ra. Внешний энергетический уровень атомов этих элементов характеризуется наличием двух спаренных s - э лектронов, следовательно, в нормальном состоянии эти элементы нульвалентны. Однако пара s - электронов их атомов при незначительной затрате энергии переходит в возбужденное состояние, при котором один s - электрон переходит на р-подуровень: s2 - s1p1 - В этом состоянии оба электрона непарны, и проявляемая этими элементами валентность становится равной двум. Радиусы атомов этих элементов меньше, чем радиусы атомов элементов соседней IA группы, а энергии ионизации соответственно больше, что характеризует их как менее активные восстановители по сравнению с группой IA. Но в этом отношении они уступают только щелочным металлам. [35]
Действие динатронного генератора основано на так назы-аемом динатронном эффекте, состоящем в том, что при попада-ии электронов на анод возникает вторичная эмиссия; электрон, рилетающий на анод из катода, выбивает из анода новые элек-роны. Если на один первичный электрон приходится несколько торичных, то составляющая тока, обусловленная вторичными лектронами, преобладает над током первичной эмиссии. В ре-ультате этого анодный ток не только убывает, но может даже зменить знак. Очевидно, что каждый первичный электрон мо-сет выбить тем больше вторичных, чем больше скорость пер-ичного электрона. Скорость же электрона зависит от ускоряю - tero напряжения. В качестве динатрона может быть использо-ан любой подходящий триод. [36]
Например, ядро атома водорода, присоеди - [ енного к а-атому углерода, создает локальное магнитное поле у лектрона, которое либо прибавляется к внешнему полю, либо вычи-ается из него в зависимости от ориентации ядерного спина. [37]
Грамм-эквивалент ( г-экв) - эквивалентный вес, выраженный в грам - iax, он соответствует ( в данной реакции) 1 грамм-атому водорода или / з грамм-атома кислорода, или 1 одновалентному грамм-иону. В окислительно-восстановительных реакциях грамм-эквивалент равен частному т деления 1 г-моля ( г-атома или г-иона) данного вещества на число лектронов, которое в данной реакции 1 молекула ( 1 атом или 1 ион) этого вещества присоединяет или отдает. [38]
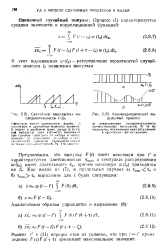 |
Квазипериодический импульсный процесс. [39] |
Импульсы имеют одинаковую форму, i: o возникают в случайные моменты времени. В задаче о дробовом шуме диода ( § 8) та-кне импульсы тока д: ( () ( 0 возникают при пролете лектрона от катода к анолу: моментк их появления случайны в силх случайности процесса термоэлектронной г также ФГ ТП ЛРКТГ-ОНЧОЙ. [40]
Предположим, что частота колебаний электрического поля, под действием которого создается этот ток, настолько велика, что за время свободного пробега э лектрона успеет произойти очень много колебаний поля. Для того чтобы определить силу тока, создаваемого переменным полем, нужно знать скорость электронов. [41]
В спектрах BrCN и C1CN а-система перекрывается системой А. Авторы [1432] показали, что Л - система связана с переходом AlYl - Xi S, причем состояние Ain образуется при промотировапии 5а - лектрона. Идентификация верхнего состояния - системы остается сомнительной. [42]
Наблюдающаяся в большинстве случаев высокая химическая активность радикалов обусловлена незаконченностью электронных оболочек соответствующих атомных групп, благодаря чему свойства этих групп приближаются к свойствам атомов, обладающих тем же количеством внешних электронов, что и данная атомная группа. В этом отношении особенно характерна аналогия между химическими свойствами гидридов углерода, азота, кислорода и фтора и химическими свойствами атомов с тем же числом н лектронов. Так, радикал СН ( метин) является химическим аналогом атома N, радикалы СН2 ( метилен) и NH ( имин) - аналогами атома О, радикалы СН3 ( метил), NH2 ( аминогруппа) и ОН ( гидроксил) - аналогами атома F и, наконец, молекулы СН4, NHs, H2O и HF в известном смысле ( инертность) аналогичны атому Ne. Благодаря химической ненасыщенности радикалов энергия активации процессов, протекающих с их участием, имеет порядок величины энергии активации атомных реакций. Поэтому эти процессы, как правило, идут приблизительно с такой же скоростью, с какой обычно идут атомные процессы. [43]
Поскольку в результате элиминирования ЭН образуется один и тот же катион, можно считать, что наблюдаемые изменения относительной интенсивности катиона с т / е 105 обусловлены в основном уменьшением прочности связи С - Э в порядке S Se Те. Частица с т / е 105 [ С8Н9 ], вероятнее всего, имеет структуру метилтропилиевого катиона, в котором происходит максимально возможная ( для данного набора ядер и лектронов) стабилизация положительного заряда. [44]
Страницы: 1 2 3 4
