Леннард-джонс
Cтраница 2
Леннард-Джонса), которая во многих случаях справедлива в широком интервале значения R. В этой формуле е и а - константы с размерностями энергии и длины соответственно. Подходящий выбор значений этих констант позволяет с довольно хорошим приближением описать экспериментально наблюдаемые свойства атомов благородных газов и двухатомных молекул, не обладающих ди-польным моментом. [16]
Леннард-Джонса, который в свою очередь, по данным опыта, довольно правильно выражает межатомное взаимодействие в жидком аргоне ( см. гл. [17]
 |
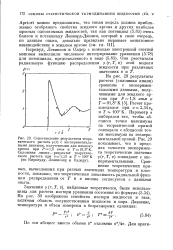
Одномерная мо-ячейки в системе из. [18] |
Леннард-Джонса и Девоншайра состоит в следующем. [19]
Леннард-Джонса, который в свою очередь, по данным опыта, довольно правильно выражает межатомное взаимодействие в жидком аргоне ( см. гл. [21]
Леннард-Джонса и что волновая функция системы дается произведением экспоненциальных функций, включающих три одинаковых для всех экспонент вариационных параметра. Так как экспериментальная энергия связи в жидком гелии составляет Еь - 9 88 - 10 - 23 Дж / атом, то авторы работы [441] заключили, что для описания свойств массивной жидкости достаточен кластер из 87 атомов. [22]
Леннард-Джонса дали результаты, хорошо согласующиеся с экспериментом. [23]
 |
Модель Леннард-Джонса. [24] |
Модель Леннард-Джонса используется во многих работах [27], [78], [82-86], в которых разработаны методы расчета не только для коэффициентов диффузии, но и для других характеристик молекулярного переноса в газовой фазе. [25]
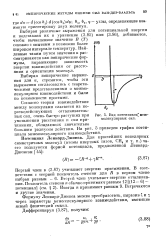 |
Вид потенциала межмолекулярных сил. [26] |
Формулу Леннард-Джонса можно преобразовать, выразив С и - j через параметры межмолекулярного взаимодействия, имеющие ясный физический смысл. [27]
Потенциал Леннард-Джонса ( первый член в правой части) учитывает отталкивательные, дисперсионные и индукционные взаимодействия. [28]
В действительности Леннард-Джонс имел в знаменателе 6 вместо 12, что является числовой ошибкой, сделавшей вычисленные им теплоты адсорбции вдвое большими. [29]
В действительности Леннард-Джонс имел в знаменателе 6 вместо 12, что является числовой ошибкой, сделавшей вычисленные им теплоты адсорбции вдвое бблыпими. [30]
Страницы: 1 2 3 4