Летучесть - растворенное вещество
Cтраница 1
Летучесть растворенного вещества с парами растворителя вызывает ошибки, аналогичные ошибкам при вымерзании с растворителем. [1]
Зависимость летучести растворенного вещества в разбавленном растворе от его состава можно найти с помощью уравнения Гиббса - Дюгема ( 1 - 89), принимая во внимание, что растворитель подчиняется закону Рауля. [2]
Рассмотрим предварительно летучесть растворенного вещества в обычных бесконечно разбавленных растворах при изменениях вдоль выбранной кривой. [3]
Nf - 0 летучесть растворенного вещества совпадает с его парциальным давлением. [4]
Летучесть растворителя значительно больше летучести растворенного вещества. Для этого, если растворимость неизвестна, оценивают ее хотя бы приблизительно, используя приемы, описанные в § 4.3. Убедившись, что растворимость удовлетворительна, для приготовления насыщенного раствора выдерживают его с избытком вещества при соответствующих температурах в течение 1 - 2 сут ( лучше взбалтывая), после чего осторожно отделяют его от осадка. Полученные таким образом растворы разливаются каждый на 4 часовых стекла примерно равными порциями. К поверхности раствора прикасаются иглой, которую предварительно заражают кристаллизуемым веществом, дотрагиваясь ею до реактива. Затем растворы на стеклах оставляются при той же температуре, при которой насыщались; при этом они прикрываются фильтровальной бумагой. Пара растворов из каждой группы поверх фильтровальной бумаги накрывается, кроме того, куском стекла для резкого замедления испарения. В зависимости от конкретных особенностей раствора ( значения растворимости, скорости испарения), что определяет скорость кристаллизации и число образующихся кристаллов, раствор оставляют на то или иное время, иногда до полного испарения. [5]
Если в уравнении ( VIII, 50) рассматривать / 2 как летучесть растворенного вещества в газовой фазе, равновесно сосуществующей с жидкой ( твердой) фазой, то уравнение ( VIII, 50) является точной термодинамической формой закона Генри. [6]
Значение этого коэффициента можно найти, измеряя или летучесть растворителя, или летучесть растворенного вещества в критических фазах вдоль начального участка критической кривой. [7]
На результаты парофазной осмометрии оказывают также влияние такие факторы, как размер капли, летучесть растворенного вещества и процессы, лимитируемые диффузией. [8]
Таким образом, в бесконечно разбавленном растворе летучесть растворителя вычисляется по закону Рауля, а летучесть растворенного вещества по закону Генри. Оба закона справедливы вне зависимости от агрегатного состояния раствора. [9]
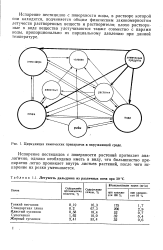 |
Циркуляция химических препаратов в окружающей среде.| Летучесть дильдрина из различных почв при 30 С. [10] |
Испарение пестицидов с поверхности воды, в растворе которой они находятся, подчиняется общим физическим закономерностям летучести растворенных веществ и растворителя; плохо растворимые в воде вещества улетучиваются также совместно с парами воды, пропорционально их парциальному давлению при данной температуре. [11]
Уравнение (II.1), написанное даже как предельное при N2, стремящемся к нулю, справедливо только в том случае, когда летучесть растворенного вещества совпадает с его парциальным давлением. Это практически всегда оправдывается в тех случаях, когда упругость насыщенного пара растворителя мала и, следовательно, газовая фаза практически является смесью идеальных газов. Для растворителя с большой упругостью пара ( например, для жидкого аммиака) даже при N2 - 0 замена летучести парциальным давлением в общем случае недопустима. [12]
Экспериментальным путем надежные данные для однозначного решения вопроса получить очень трудно. Экспериментальные трудности связаны с тем, что в разбавленных растворах летучесть растворенного вещества очень мала и тем более трудным является исследование зависимости этой малой величины от концентрации раствора. [13]
Растворы иода необходимо стандартизировать каждые несколько дней. Малая устойчивость его растворов объясняется несколькими причинами, одна из них - летучесть растворенного вещества. Даже если взять большой избыток иодида, заметное количество иода теряется из открытого сосуда за относительно короткий период времени. [14]
 |
Схема кристаллизации смеси двух веществ ( на рисунке вместо р к2 следует читать р 2Ка. [15] |
Страницы: 1 2