Замерзание - чистая вода
Cтраница 2
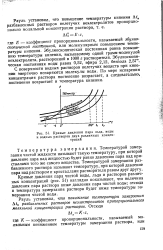 |
Кривые давления пара льда, воды. [16] |
Кривые давления пара чистой воды, льда и растворов различных концентраций ( рис. 51) наглядно показывают, что величина давления пара раствора ниже давления пара чистой воды; отсюда и температура замерзания раствора будет ниже температуры замерзания чистой воды. [17]
Кри-осохранение в буквальном смысле Означает хранение в замороженном состоянии. Точка замерзания чистой воды соответствует 0 С, точка переохлаждения, или образования однородных центров кристаллизации соответствует - 38 С. Сохраняемый биообъект переходит в анабиотическое состояние, когда метаболизм замедляется или приостанавливается на время хранения. При этом также не происходят какие-либо генетические изменения за исключением повреждающего действия ионизирующей радиации. [18]
 |
Схема определения связи осмотического давления раствора с давлением насыщенного пара. [19] |
Всякая жидкость начинает замерзать при той температуре, при которой она будет иметь такое же давление пара, как и твердые кристаллы этой жидкости. Эта температура и является точкой замерзания чистой воды. [20]
Вымораживание основано на использовании явления разделения кристаллов пресного льда и рассола при замерзании соленой воды. Температура замерзания рассола ниже температуры замерзания чистой воды и зависит от концентрации солей. Поэтому в твердое состояние вначале переходит чистая вода, а рассол в виде вакуолей оказывается включенным в массу пресного льда. [21]
 |
Растворимость Na2SO4 в воде ( вес 96. [22] |
Для того, чтобы исключить применение пространственной модели, в ней выделяют плоскость постоянного давления или поверхность собственного давления водяного пара, которую затем ортогонально проектируют на координатную плоскость температура - концентрация, получая двухмерную проекцию, удобную для расчетов. На обоих рисунках точка 0 отвечает температуре замерзания чистой воды, а кривые PQ, MN и 0 Р температуре и составу растворов, находящихся в равновесии с одной твердой фазой: Na SC. [23]
При абсолютном нуле кинетическая энергия равна нулю. На шкале Цельсия ( С) за 0 принята точка замерзания чистой воды при стандартных условиях. [24]
Точка льда находится ниже тройной точки воды на 0 00980 С. При этом понижение на 0 00743 С обусловлено зависимостью точки замерзания чистой воды от давления, а понижение на 0 00237 С вызывается растворенным в воде воздухом. [25]
Во влаге, содержащейся в пищевых продуктах, растворены различные минеральные и органические вещества. Поэтому образование льда происходит при постепенном понижении температуры в отличие от изотермического замерзания чистой воды. [26]
Температура замерзания морской воды равна 271 240 К. Определите осмотическое давление морской воды при температуре около 273 К, если температура замерзания чистой воды составляет 273 150 К, молярный объем воды равен 18 мл / моль, а молярная энтальпия таяния льда равна 6000 Дж / моль. [27]
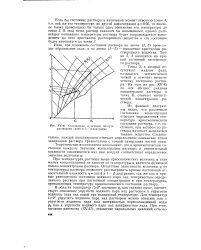 |
Охлаждение и осушка воздуха растворами солей в / - d - диаграмме. [28] |
Из фазовой диаграммы видно, что различным состояниям концентрации отвечает определенная температура криоскопического состояния раствора, т.е. состояния, при котором из раствора начинает выделяться твердое вещество. Следовательно, каждой концентрации отвечает определенное понижение точки замерзания раствора сравнительно с точкой замерзания чистой воды. [29]
Жидкость начинает замерзать при той температуре, при которой она будет иметь такое же давление пара, как и твердые кристаллы этой жидкости. Точке А соответствует температура О С. Эта температура и является точкой замерзания чистой воды. [30]
Страницы: 1 2 3