Замещение - молекула - вода
Cтраница 2
К полученному раствору прибавляют небольшими порциями 20 г кристаллического нитрита натрия и нагревают смесь на кипящей водяной бане до появления буровато-желтой окраски, что указывает на замещение молекул воды во внутренней сфере нитритными группами. [16]
Ионы водорода не вытесняются. Реакция координации происходит в результате замещения молекул воды нейтральными молекулами реагента. Следовательно, продукт представляет собой катион с той же зарядностью, что и исходный ион металла. Хотя продукт обычно растворим в воде, но иногда он поддается экстракции органическими растворителями - вследствие наличия необычайно массивного катиона и подходящих анионов. Так, соли Си1 и Fe11 с производными 1, 10-фенантролина можно экстрагировать5 такими растворителями, как высшие спирты. [17]
Иначе говоря, при образовании ионной пары не происходит замещения молекул воды, соль-ватирующих ион металла, или других групп, непосредственно окружающих его. С другой стороны, процесс комплексообразо-вания, протекающий в водном растворе, предусматривает частичное или полное замещение молекул воды, непосредственно окружающих ион металла, на одну или несколько молекул лиганда. Если получающийся в результате этого комплекс не имеет заряда и не содержит гидрофильных групп, можно ожидать, что он будет мало растворим в воде. [18]
Ранее уже было отмечено, что ионы водорода и гидроксила занимают особое положение в том смысле, что они могут реагировать с другими ионами в воде по специальному механизму, не требующему удаления сольватирующих молекул воды. Любая другая реакция ассоциации какого-нибудь иона требует удаления и замещения молекулы воды в координационной сфере. [19]
До сих пор при обсуждении процессов в растворах не учитывалось влияние близкодействующих сил, в результате действия которых происходит обмен электронов. Одновременно с этим процессом или вместо него может происходить замещение молекул воды другими лигандами. [20]
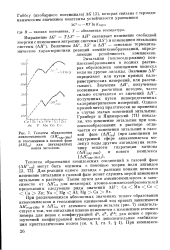 |
Теплоты образования аквакомплексов ( ДН. идр ( Ме и гексамминов в газовой фазе ДН. аз для двухзарядных ионов металлов. [21] |
Величины AG, A610 и ДЯ - основные термодинамические характеристики реакций комплексообразования, определяющие устойчивость комплексов. Энтальпия ( теплосодержание) комплексообразования в водных растворах обусловлена замещением молекул воды на другие лиганды. Значение ДЯ определяют или путем прямых калориметрических измерений, или рассчитывают. Значения ДЯ, полученные косвенным расчетным методом, часто сильно отличаются от значений ДЯ0, полученных путем непосредственных калориметрических измерений. Однако прямой метод практически не применим в случае малых изменений энтальпии. [22]
Величины ДС, До10 и ДЯ - основные термодинамические характеристики реакций комплексообразования, определяющие устойчивость комплексов. Энтальпия ( теплосодержание) комплексообразования в водных растворах обусловлена замещением молекул воды на другие лиганды. Значение ДЯ определяют или путем прямых калориметрических измерений, или рассчитывают. Значения ДЯ, полученные косвенным расчетным методом, часто сильно отличаются от значений ДЯ, полученных путем непосредственных калориметрических измерений. Однако прямой метод практически не применим в случае малых изменений энтальпии. [24]
Считают, что хелатный эффект связан с изменением энтропии системы. При образовании комплексов, например в водном растворе, происходит замещение молекул воды гидратированного иона металла на определенный лиганд. [25]
Необходимо также знать, при какой концентрации аква-ион элемента находится в мономерной форме. Сведения о КуСТ аква-комплексов изучаемого иона элемента и их способности к замещению молекул воды на другие лиганды ( их инертности) можно получить, главным образом, из периодической литературы; число таких работ пока не очень велико. [26]
Сольватирующее действие экстрагента, в данном случае ТБФ, основано на замещении молекул воды в координационной сфере металла. Роль соль-ватирующего агента может выполнять и сам органический растворитель, применяемый для экстракции. Такими свойствами обладают спирты, кетоны, эфиры ( или тот же ТБФ, если его использовать в неразбавленном виде), которые легко координируются металлами благодаря высокой электронной плотности на атоме кислорода, а также амины, соли четвертичных аммониевых и аналогичных им оснований. Так, при экстракции Co ( SCN) 4 - из слабокислой среды пентиловым спиртом координированные молекулы воды замещаются на молекулы спирта, и соединение легко переходит в органическую фазу. На этом основано увеличение чувствительности качественной реакции кобальта ( II) с тиоцианатом ( эффект смещения равновесия реакции и концентрирования, см. гл. [27]
Необходимо также знать, при какой концентрации аква-ион элемента находится в мономерной форме. Сведения о / Суст аква-комплексов изучаемого иона элемента и их способности к замещению молекул воды на другие лиганды ( их инертности) можно получить, главным образом, из периодической литературы; число таких работ пока не очень велико. [28]
Устойчивость соединения к окислению авторы объясняют тем, что электроны, образующие связь между атомами родия, экранируются циклами ацетата и при воздействии окислителей не меняют своего положения. При действии на [ Rh - ( СН3СОО) 2Н2О ] 2 аммиака, пиридина и ацетамида происходит замещение молекул воды соответствующим амином. Ацетат-ион при этом не замещается. [29]
ФЭП), а возможно, и с р-фосфатом АТФ и АДФ. Однако добавление ФЕП к Е - Мп приводит к гораздо большим изменениям в усилении релаксации, чем в тех случаях, когда это можно объяснить простым замещением молекулы воды. Вероятно, свой вклад в это явление вносят и конформационные изменения фермента. [30]
Страницы: 1 2 3