Заряд - электрод
Cтраница 1
Заряд электрода означает наличие вблизи его поверхности неэквивалентного количества подвижных электронов и сопровождающих их положительных ионов; противоположный заряд образуется избытком одного типа ионов в окружающем растворе. Аналогия подобной системы с плоскопараллельным конденсатором, использованная Гельмгольцем [1], лежит в основе современной теории двойного слоя. Однако в отличие от плоскопараллельного конденсатора разность потенциалов между обкладками двойного слоя не равна нулю при потенциале нулевого заряда вследствие разделения других видов заряда в каждой фазе - электроде и электролите. Поэтому простое измерение потенциала не указывает заряд электрода. [1]
Заряд электрода увеличивается также при вылете заряженных частиц с его поверхности, покрытой активным веществом. [2]
Заряд электрода сопровождается концентрационной поляризацией, обусловленной изменением состава вещества в реакционной зоне как в твердой фазе, так и в электролите. Выравнивание состава более окисленной массы активного вещества, находящегося в поверхностном слое частиц, и менее окисленного вещества, находящегося в глубине частиц, происходит за счет Диффузии протонов в твердой фазе из глубинных слоев к поверхности. Этот процесс протекает с небольшой скоростью. [3]
 |
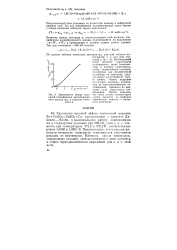
Схема капиллярного алектрометра Гун. [4] |
Заряд электрода является функцией потенциала электрода и степени заполнения поверхности электрода молекулами адсорбата. [5]
Заряд электрода из окиси серебра током, периодически меняющим направление. [6]
Заряд электрода, если последний изготовлен из металла, стоящего в ряду активностей после водорода, будет отрицательным, до водорода - положительным. [7]
Заряд электрода находят: а) из электрокапиллярных кривых, применяя уравнение ( 11) гл. [8]
Заряд электрода при постоянной концентрации раствора, постоянной температуре и давлении является функцией только потенциала и относительного поверхностного избытка адсорбированных частиц. [9]
Заряд электрода в том случае, если он изготовлен из металла, стоящего в ряду активности после водорода, будет отрицательным, а стоящего до водорода - положительным. В практике потенциометрических анализов измерение электродных потенциалов производится по отношению к определенным электродам сравнения, нормальные потенциалы которых известны. [10]
Величина заряда электрода q, соответствующая этой величине специфически адсорбированного заряда, подсчитывается по выражению - 7 / Т FT и приведенным в условии задачи ( табл.) данным. [12]
 |
Схема измерительной установки в кулонометрическом методе. [13] |
Плотность заряда электрода изменяется за весьма малый промежуток времени ( 0 1 - 1 мкс), за это время достигается r mai, после чего перенапряжение постепенно падает до нуля. [14]
При заряде электрода вся содержащаяся в нем окись цинка может быть восстановлена до металлического цинка. [15]
Страницы: 1 2 3 4