Заряд - ядро - атом
Cтраница 1
Заряд ядра атома равен сумме зарядов 11 протонов, находящихся в ядре, масса которых равна 11 УЕ. Так как массовое число натрия равно 23 УЕ, то разность 23 - 11 12 определяет число нейтронов в атоме натрия. [1]
Заряд ядра атома равен сумме зарядов 11 протонов, находящихся в ядре, масса которых равна 11 УЕ. Так как массовое число натрия разно 23 УЕ, то разность 23 - 11 12 определяет число нейтронов в атоме натрия. [2]
Заряд ядра атома равен сумме зарядов 11 протонов, находящихся в ядре, масса которых равна S1 УЕ. Так как массовое число натрия равно 23 УЕ, то разность 23 - 11 12 определяет число нейтронов в атоме натрия. [3]
Заряд ядра атома и суммарный заряд электронов, вращающихся вокруг ядра, одинаковы по величине, но различны по знаку. Поэтому атом в целом не имеет заряда; он электронейтрален. [4]
Заряд ядер атомов увеличивается. [5]
Заряд ядра атома, определенный в работах Мозли, Резерфорда и Чэдвика и совпадающий с порядковым номером, присвоенным данному элементу Д. И. Менделеевым ( Ван-дер - Брук), одновременно определяет число электронов в данном атоме в силу нейтральности атомной структуры. [6]
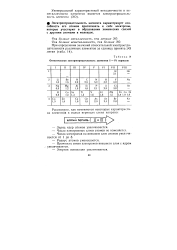 |
Относительная электроотрицательность элементов 1 - IV период. ов. [7] |
Заряд ядер атомов увеличивается. [8]
Заряд ядра атома, определенный в работах Мозли, Резерфорда и Чадвика и совпадающий с порядковым номером, присвоенным данному элементу Д. И. Менделеевым ( Ван-дер - Брук), одновременно определяет число электронов в данном атоме в силу нейтральности атомной структуры. [9]
Заряд ядра атома 2 является основной характеристикой, определяющей индивидуальность элемента. [10]
 |
Схемы строения атома и иона магния.| Схемы строения атома и иона кислорода. [11] |
Заряд ядра атома при всех химических реакциях, в которых участвует данный элемент, остается неизменным. [12]
Заряд ядра атома характеризует элемент точнее, чем атомный вес, определяемый обычными химическими методами. [13]
 |
Баланс круговорота азота в биосфере. [14] |
Заряд ядра атома фосфора достаточно велик ( Z 15), чтобы вызывать магнитные силы, действующие даже при обычных температурах каталитически на химические процессы весьма замедленного действия, присущие молекулам таких легких атомов, как Н, С, N и О. Характерным примером могут служить реакции при обычной температуре в случае сходных соединений элементов 2-го и 3-го периодов - действие воды на СС14 и на SiCl 4: только последнее из этих соединений очень быстро подвергается гидролизу. [15]
Страницы: 1 2 3 4