Анодное кривое заряжение
Cтраница 1
Анодные кривые заряжения, снятые после восстановления хемо-сорбированных частиц, в случае нитрометана не совпадают с кривой фона, что свидетельствует о наличии на электродах невосстанавливаемых частиц, занимающих от 5 до 17 % поверхности. [1]
Анодные кривые заряжения показывают, что образующиеся гидридные соединения покрывают значительную часть поверхности электрода. Поэтому, вероятно, что процесс выделения водорода на кремнии проходит через стадию образования таких гидридов. [2]
На анодных кривых заряжения практически отсутствует влияние хлорофоса в меньшей концентрации при малой i и слабое облагораживание большей добавкой. При i 30 ма / см2 анодный процесс тормозится тем сильнее, чем больше добавка хлорофоса. [3]
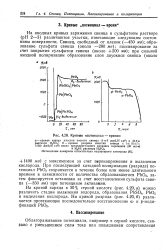 |
Кривые потенциал - время. [4] |
На анодных кривых заряжения свинца в сульфатном растворе ( рН 2 - 3) различаются участки, отвечающие следующим состояниям поверхности. [5]
Осциллографическая запись анодных кривых заряжения показывает, что в чистом растворе хлорида электрод находится в активно-пассивном состоянии ( рис. 1 3); наблюдающиеся осцилляции потенциала связаны с тем, что на электроде протекают два конкурирующих процесса - активация и пассивация. Если в электролит добавить нитрат - или сульфат-ионы, потенциал электрода стабилизируется, осцилляции прекра - Рис 12 - Влияние добавок посто. [6]
С исследуемого электрода при; помощи осциллографа снимались анодные кривые заряжения в растворе 10 % - ной НС1 20 С), когда палладий анодно растворяется, а основной металл ( титан или нержавеющая сталь) находится в пассивном состоянии. [8]
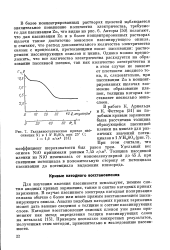 |
Гальваностатическая кривая пас - пленки на никеле для раз. [9] |
Для изучения явления пассивности используют, помимо снятия анодных кривых заряжения, также и снятие катодных кривых заряжения. В случае пассивного электрода катодная поляризация связана обычно с более или менее прямым восстановлением пассивирующего окисла. Анализ подобных катодных кривых заряжения может дать важные сведения о толщине и составе пассивирующих слоев. Приведем несколько конкретных результатов, полученных этим методом, применительно к исследованию пассивности. [10]
В последней работе [153] было показано, что на катодных и анодных кривых заряжения платины, палладия и золота имеется задержка порядка 10 3 мкк / см2 и потенциалы, отвечающие середине задержки, смещаются на 59 мв при изменении рН на единицу. [11]
ОН и Pt - О, Данные, полученные методом треугольных импульсов напряжения, трудно интерпретировать с точки зрения равновесной адсорбционной емкости, поскольку и ток, и потенциал не являются постоянными, а катодные и анодные кривые заряжения необратимы. Это не позволяет использовать для анализа таких случаев окисления теоретические подходы, описанные в предыдущих разделах. [12]
Каждую анодную и соответствующую ей катодную кривую заряжения строят на отдельном графике. Для всех полученных анодных кривых заряжения находят среднее значение С. [13]
I, 2 /, не меняется с переходом к сплавам с невысоким содержанием Ru и Pt и что реакция растворения можно пренебречь. Количества электричества, использованные в расчете, взяты из четко выраженных на анодных кривых заряжения задержек, предшествующих области потенциалов, которая связана с началом разряда С1 - - иона. [14]
На рис. 1 представлены зависимости изменения толщин окисных слоев на электродах из сплавов Tt с Ru ( кривая I) и Тс с P-i ( кривая 2) от концентрации активной компоненты в сплаве, рассчитанных для каждого из сплавов по анодным кривым заряжения из предположений, что фактор шероховатости 2 5, общепринятый для Tt / I, 2 /, не меняется с переходом к сплавам с невысоким содержанием Ru и Pi и что реакциями растворения можно пренебречь. Количества электричества, использованные в расчете, вачты из четко выраженных на анодных кривых заряжения задержек, предшествующих область-потенциалов, которая связана с началом разряда С1 - - иона. [15]
Страницы: 1 2
