Значение - катодный потенциал
Cтраница 1
 |
Значение катодного потенциала на графитовых электродах ( в мВ.| Зависимость анодного ( Еа и катодного ( Ек потенциалов от плотности тока на графитовых электродах. [1] |
Значения катодного потенциала существенно изменяются при переходе от одного процесса к другому. [2]
При этом значение катодного потенциала возрастает до величины, необ - - ходимой для разряда ионов водорода. [3]
 |
Каталитическое влияние материала электрода. [4] |
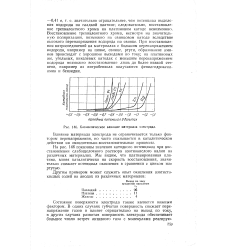
На рис. 146 показаны значения катодного потенциала при восстановлении слабощелочного раствора азотнокислого калия на различных материалах. Мы видим, что платинированная платина, влияя каталитически на скорость восстановления, значительно снижает потенциал окисления в сравнении с цинком или ртутью. [5]
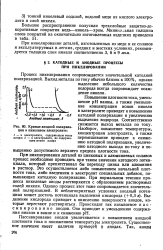
На рис. 2 нанесены значения установившегося катодного потенциала фк за вычетом омической составляющей. Начальный и конечный участки суммарной поляризационной кривой ( рис. 2, кривая /) свидетельствуют о небольшом увеличении ф с ростом DK, средний участок отличается значительной поляризацией. [6]
В табл. 53 приведены измеренные177 значения катодного потенциала на графитовых электродах в процессах прямого электролиза соляной кислоты и электролиза солянокислых растворов хлоридов меди и ртути. [7]
При построении первой кривой на оси абсцисс откладывают значения катодного потенциала, а на оси ординат - плотность тока. Построив график т ] н - Igi, определяют коэффициенты а и Ъ в уравнении Тафеля. [8]
Если электролиз проводят в таких условиях, которые обеспечивают значение катодного потенциала, соответствующего точке на участке предельного тока ( см. рис. 14 - 5), то сила тока определяется скоростью переноса массы. При данных условиях электролиза ( состав ванны, расположение электродов, перемешивание раствора) предельный ток - это максимальный ток, который может проходить при 100 % - ном выходе металла на катоде по току. Следовательно, применяя прибор, поддерживающий постоянный катодный потенциал, независимый от колебаний силы тока и изменений анодного потенциала, при заданных условиях можно достигнуть наибольшей возможной скорости осаждения и к тому же избежать возникновения побочных реакций на катоде. При этом, поскольку выделение водорода исключено, металл осаждается гладким компактным слоем, что особенно ценно при электрогравиметрических определениях. [9]
При никелировании деталей из цинковых и алюминиевых сплавов процесс необходимо проводить при таком значении катодного потенциала, который препятствовал бы переходу цинка или алюминия в раствор. Это осуществляется либо повышением начальной плотности тока, либо введением в электролит специальных добавок, повышающих катодную поляризацию. При нормальном течении процесса никелевые аноды растворяются с образованием растворимых солей никеля. Однако процесс этот тоже сопровождается значительной поляризацией. Выделение кислорода приводит к окислению поверхности анодов, которые перестают растворяться. Происходит так называемое пассивирование анодов. [10]
 |
Кривые анодной поляризации в никелевом электролите. [11] |
При никелировании деталей из цинковых и алюминиевых сплавов процесс необходимо проводить при таком значении катодного потенциала, который препятствовал бы переходу цинка или алюминия в раствор. Это осуществляется либо повышением начальной плотности тока, либо введением в электролит специальных добавок, повышающих катодную поляризацию. При нормальном течении процесса никелевые аноды растворяются с образованием растворимых соле й никеля. Однако процесс этот тоже сопровождается значительной поляризацией. Выделение кислорода приводит к окислению поверхности анодов, которые перестают растворяться. Происходит так называемое пассивирование анодов. [12]
Пусть электровосстановление какого-либо соединения на разных металлах проводится при одном и том же значении катодного потенциала, например при - 0 8 В по водородной шкале. В качестве катодов используются ртуть, свинец, цинк и серебро. Все эти металлы относятся к первой электрохимической группе и, следовательно, не отличаются друг от друга природой восстанавливающего агента. Однако и в этом случае условия протекания реакции на каждом из металлов при одном и том же катодном потенциале оказываются различными. Это различие связано с тем, что ни их заряды, ни степень адсорбции восстанавливаемого вещества не совпадают по своему значению. Нулевые точки ( см. табл. 11.6) равны для ртути - 0 2, для свинца - 0.7, для цинка - 0 5 В. [13]
Пусть электровосстановление какого-либо соединения на разных металлах проводится при одном и том же значении катодного потенциала, например, при - 0 8 в по водородной шкале. В качестве катодов используются ртуть, свинец, цинк и серебро. Все эти металлы относятся к первой электрохимической группе и, следовательно, не отличаются друг от друга природой восстанавливающего агента. Однако и в этом случае условия протекания реакции на каждой из металлов при одном и том же катодном потенциале оказываются различными. Это различие связано с тем, что ни их заряды, ни степень адсорбции восстанавливаемого вещества не совпадают по своей величине. [14]
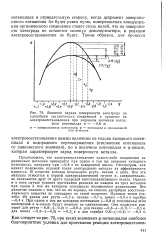 |
Влияние заряда поверхности электрода на адсорбцию органических соединений в процессе их электровосстановления при заданном значении катодного потенциала е - 0 8 в. [15] |
Страницы: 1 2