Анион - сильная кислота
Cтраница 2
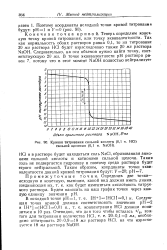 |
Кривая титрования сильной кислоты ( 0 1 н. НС1 сильной щелочью ( 0 1 н. NaOH. [16] |
NaCl, образованная анионами сильной кислоты и катионами сильной щелочи. Такая соль не подвергается гидролизу и поэтому среда раствора будет строго нейтральной. [17]
Соли катионов с анионами сильных кислот чаще всего хорошо растворимы в воде. [18]
В отличие от них анионы сильных кислот, как, например, ион NO3, не проявляют сильных основных свойств, способных вызвать реакцию гидролиза, а поэтому не влияют на рН раствора. [19]
Для вод с содержанием анионов сильных кислот 6 - 7 мг-экв / кг количество сбросных вод при глубоком химобессоливании превышает сбросы при использовании таких же испарителей уже в 10 раз. Количество сбросных вод при использовании испарителей, питаемых водой, прошедшей упрощенную обработку ( подкисление, содоизвесткование или известкование) ( кривая 3), еще меньше. [20]
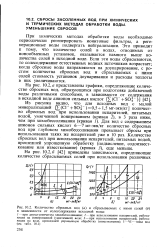 |
Количество сбросных вод ( а и сбрасываемых с ними солей ( б в зависимости от солесодержания исходной воды. [21] |
Для вод с содержанием анионов сильных кислот 6 - 7 мг-экв / кг количество сбросных вод при глубоком химобессоливании превышает сбросы при использовании таких же испарителей уже в 10 раз. Количество сбросных вод при использовании испарителей, питаемых водой, прошедшей упрощенную обработку ( подкисление, содоизвест-кование или известкование) ( кривая 3), еще меньше. [22]
После поглощения определенного количества анионов сильных кислот дальнейшая способность низкоосновного анионита извлекать их из воды исчерпывается, и становится необходимой его регенерация, достигаемая - пропусканием через фильтр раствора щелочи. [23]
Наличие в их молекуле аниона сильной кислоты обеспечивает диссоциацию и соответственно хорошее моющее действие таких ПАВ как в щелочной, так и в кислой среде, а также в жесткой воде. [24]
К обменным реакциям с анионами сильных кислот способны как сильноосновные, так и слабоосновные аниониты, основность которых определяет типы привитых функциональных групп. [25]
Если осадок MmAn образован анионом сильной кислоты и катионом слабого основания, то при его растворении происходит протолиз катиона, который сопровождается образованием различных гидроксокомплексов и увеличением растворимости осадка. [26]
Если окрашенное соединение образовано анионом сильной кислоты, как, например, при определении висмута в виде иодидного комплекса, то реакцию обычно-проводят при постоянной концентрации реактива и в довольно кислой среде, обеспечивающей подавление гидролитических процессов. Концентрация аниона в таких системах от кислотности среды не зависит. При использовании в качестве реагента слабой кислоты, например при определении железа в виде сульфосалицилатного комплекса, рН раствора должен находиться в слабокислой области, в которой диссоциация кислоты достаточна и концентрация реактива постоянна. Особое внимание должно быть уделено постоянству рН во всех исследуемых растворах. [27]
Фторосульфонатный анион, будучи анионом сильной кислоты, образует нормальные соли с электроположительными металлами. Имеются многочисленные сообщения о смешанных фторо-сульфонатных производных галогенидов металлов, которые, видимо, являются двойными солями. Были опубликованы результаты исследований инфракрасных спектров [83] и спектров комбинационного рассеяния [84] этого аниона. [28]
Отметим, что катион и анион сильных кислот и основания, по существу, инертны и не принимают участия в кислотно-основных реакциях. [29]
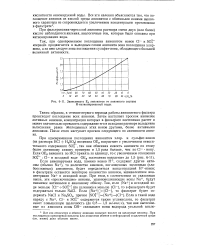 |
Зависимость Ер анионитов от анионного состава Н - катионированной воды. [30] |
Страницы: 1 2 3 4