Больший анион
Cтраница 2
Выбор этой системы был основан на предпосылке, что вероятность адсорбции больших анионов должна быть меньше, чем растворенного кислорода, и тем самым создается менее устойчивая пассивность. [17]
Аналогичное рассмотрение показывает, что стабильность солей с комплексными катионами наибольшая при больших анионах. [18]
Грегор, Белл и Маркус [23], например, утверждали, что поскольку большие анионы принято считать негидратированными, то обнаруженный ими эффект уменьшения объема трихлораце-татной смолы по сравнению с ацетатной формой можно хорошо объяснить, если допустить, что первая смола склонна к образованию ионных пар. Даже n - толуолсульфоформа набухала меньше, чем ацетатная, - в согласии с известной ван-дер-ваальсов-ской сорбцией ароматических ионов. [19]
Грегор, Белл и Маркус [23], например, утверждали, что поскольку большие анионы принято считать негидратированными, то обнаруженный ими эффект уменьшения объема трихлораце-татной смолы по сравнению с ацетатной формой можно хорошо объяснить, если допустить, что первая смола склонна к образованию ионных пар. Даже л-толуолсульфоформа набухала меньше, чем ацетатная, - в согласии с известной ван-дер-ваальсов-ской сорбцией ароматических ионов. [20]
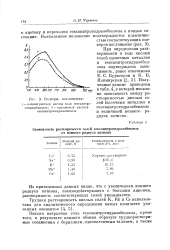 |
Спектры поглощения. [21] |
Из приведенных данных видно, что с увеличением ионного радиуса катиона, взаимодействующего с большим анионом, растворимость соответствующих солей уменьшается. [22]
Такие комплексы, как [13] -, устойчивы в растворах, но большинство полигалогенидных ионов, особенно большие анионы, существуют только в твер дых соединениях с крупными катионами. [23]
Наряду с галогенид-ионами электронными мостиками могуг быть цианид - и сульфат-ионы, молекулы воды и даже сравнительно большие анионы карбоновых и дикарбоновых кислот. [24]
Другой предельный случай ( 2) дожен осуществляться при взаимодействии очень малых по размеру катионов и очень больших анионов, как, например, Lil и MgTe среди галогени-дов элементов I группы и халькогенидов элементов II группы соответственно. В действительности же структурный тип NaCl характерен для большинства соединений этих двух семейств. Для них отношение ионных радиусов ГА: гх изменяется в очень широких пределах, и сюда входят даже такие соединения, как K. F п ВаО, которые построены из катионов и анионов приблизительно одинакового размера. Концепция ионных радиусов обсуждается в гл. [25]
Промежуточное место занимают соли четвертичных аммониевых оснований, с малыми анионами и соли третичных аммониевых оснований, с большими анионами. [26]
 |
Кислотность углеводородов по Мак-Ивену. [27] |
Полное качественное соответствие между данными Мак-Ивена в бензоле и Конанта и Уэланда в эфире означает, что стабильность этих больших анионов с рассредоточенным зарядом не очень чувствительна к природе растворителя. Дальнейшее подтверждение этого было найдено при изучении кислотности в циклогексиламине. [28]
Из диаграммы ясно, что соли с большими катионами и малыми анионами хорошо растворимы, соли с малыми катионами и большими анионами плохо растворимы. Конечно, это только очень приблизительная качественная картина растворимости. [29]
В процессе гидролиза солей коагулянтов и формирования коагулирующих коллоидных частиц гидроксидов алюминия и железа доступность внутренней поверхности пористых частиц для мицелл и больших анионов ПАВ резко сокращается. Как видно из рис. 61, уже за первые 20 - 40 с доступная удельная поверхность гидро-ксида алюминия, образующегося в результате гидролиза сульфата алюминия, сокращается в два-три раза. В дальнейшем в течение многих часов доступная удельная поверхность хлопьев гидрокси-да остается практически неизменной. Однако при высыхании хлопьев гидрогеля частицы испытывают сильное сжатие под действием капиллярных сил и доступность пор для мицелл ПАВ в результате сжатия геля понижается. [30]
Страницы: 1 2 3 4
