Бромистый изоамил
Cтраница 1
Бромистый изоамил - бесцветная жидкость, которая не растворяется в воде, легко растворяется в спирте и эфире. [1]
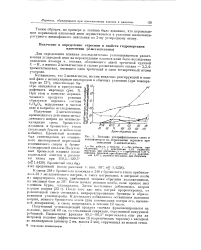 |
Влияние ультрафиолетового света и. [2] |
Бромистый изоамил был синтезирован из очищенного многократной перегонкой изоамилового спирта и броми-стоводородной кислоты. [3]
Из бромистого изоамила, магния и эфира готовят магнийорганическое соединение и к смеси в атмосфере водорода добавляют средний эфир угольной кислоты. Продукт реакции разлагают вод и и разбавленной соляной кислотой, эфир изокапроновой кислоты извлекают эфиром и фракционируют. [4]
При получении бромистого изоамила избыток брома и фосфора не должен превышать 10 % от теоретически вычисленного. [5]
При получении бромистого изоамила слишком большой избыток серной кислоты может вызвать заметное разложение. [6]
В сухую круглодонную колбу помещают бромистый изоамил, вносят туда же разрезанный на кусочки металлический натрий, закрывают пробкой с обратным воздушным холодильником и нагревают несильным пламенем горелки до начала реакции. Реакция протекает медленно, поэтому целесообразно реакционную массу оставить на сутки, после чего перенести жидкость в колбу Вюрца и разогнать. Фракция 155 - 165 С содержит основной продукт реакции - диизоамил ( темп. [7]
 |
Содержание ароматических углеводородов в каталнзате. [8] |
Диизоамил получен по Вюрцу из бромистого изоамила. [9]
По описанной выше методике проводится синтез бромистого изоамила и бромистого пропила. [10]
Исходный 2 7-диметилоктан синтезирован действием металлического натрия на бромистый изоамил. Последний готовился обычным путем из изоамилового спирта. Так как изоамиловый алкоголь брожения содержит обычно примесь оптически активного амилового спирта ( 2-метилбутанола - 1), имевшийся в нашем распоряжении препарат предварительно многократно фракционировался на колонке Гемпеля. Приготовленный из него бромид, также подвергнутый тщательной фракционной разгонке, имел т-ру кип. [11]
Равновесная система изомерных бромюров, получающаяся при нагревании до 180 - 220 бромистого изоамила, оказывается уже значительно более сложной, чем в других предыдущих случаях. [12]
Как показали М. С. Малиновский и Федосеев13, высшие бромистые алкилы ( бромистый бутил, бромистый изоамил) в кипящем эфире не вступают во взаимодействие с магнийбромацети-леном. С небольшим выходом ( 9 - 12 %) реакцию удается, однако, осуществить при более высокой температуре. [13]
Принимая во внимание данные, полученные при нагревании бромпропанов и бромизобутапов, здесь при бромистом изоамиле нужно было ожидать не только превращения исходного бромюра в третичный бро-мюр, но и обратного процесса. Кроме того, принимая механизм процесса как результат распадения бромюра при нагревании па амилен и бромистый водород и допуская, что при распадении бромистый водород может выделяться в обоих возможных направлениях, мы должны ожидать при нагревании одного из монобромизопентанов образования равновесной смеси, содержащей все четыре теоретически возможных изомерных бромизопен-тана. [14]
Таким способом получают нормальный бромистый бутил из н-бутилового спирта, красного фосфора и брома; бромистый изоамил из изоамило-вого спирта, красного фосфора и брома; йодистый этил из этилового спирта, красного фосфора и иода; йодистый нормальный амил из н-амилового спирта, фосфора и иода; йодистый изопропил из глицерина, фосфора и иода. [15]
Страницы: 1 2 3