Изобара - растворимость
Cтраница 1
 |
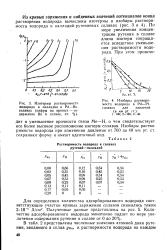
Изобары растворимости СаС12 в зависимости от температуры. [1] |
Реальные изобары растворимости отражают сочетание влияния упомянутых двух факторов. Резкое изобарическое понижение плотности пара по мере повышения температуры 600 650 ПРИ сверхкритических давлениях, но в околокритической области ( сравнить рис. 1 - 8 и рис. 6 - 1) приводит к тому, что растворимость в паре любых полярных соединений с ростом температуры падает, а одновременное уменьшение энергии кристаллической решетки несколько тормозит этот процесс. Уменьшение растворимости с ростом температуры доходит до некоторого минимального значения Смит при котором возникает перегиб кривой растворимости. С дальнейшим ростом температуры растворимость начинает увеличиваться. [2]
Изобара растворимости водорода в уране ( рис. 36) показывает, что равновесное содержание водорода в фазе a - U составляет около 1 6 - 10 - 4 вес. Однако по мере достижения последующих модификаций растворимость скачкообразно повышается. Превращение а - - 3 при 660 повышает раство-ри / мо сть с 2 до 8 - Ю-4 вес. В с луЧае расплавления урана при 1133 наблюдается значительный скачок растворимости с 17 до 28 10 - 4 вес. [3]
 |
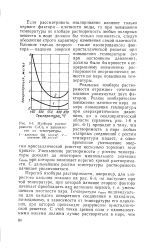
Изобары растворимости систем Сг - Н и Мо - Н для 1 атм. [4] |
Изобары растворимости системы хром - водород и молибден - водород для давления 1 атм, изученные Мартином [368] и Люкенмейером-Гассе и Шенком [369] в интервале пример-о 300 - 1200 ( рис. 58), имеют характер, обычный для случая эндотермического поглощения водорода. Для 400, 800 и 1200е растворимость водорода составляет, соответственно, 0 13; 0 44 и 2 6 - Ю-2 ат. [5]
Изобары растворимости водорода при изменении давления от 760 до 40 мм рт. ст. сохраняют форму и имеют идентичный вид. [7]
Аналогичное изменение хода изобар растворимости по достижении определенной величины давления наблюдается и в других изученных системах. [8]
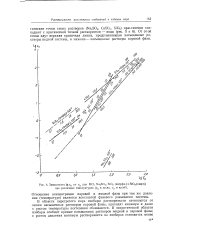 |
Зависимость lg сп от уп Для КС1, Na2SO4, SiO2 ( аморфн. и SiO2 ( кварц при различных температурах ( сп в мг / кг, уп в кг / л3. [9] |
В области перегретого пара изобары растворимости начинаются от линии насыщенных растворов паровой фазы, проходят минимум и далее с ростом температуры постепенно сближаются. [10]
Следует отметить, что уравнение изобары растворимости впервые было предложено проф. [11]
Дополнительные данные можно получить путем изучения изобар растворимости, с помощью которых определяется тепловой эффект ЛЯ. Растворимость двухатомных газов в ряде металлов увеличивается с ростом температуры, что указывает на эндотермический характер процесса. [12]
Полученные данные были интерполированы и сглажены построением изобар растворимости в координатах логарифм концентрации - обратная температура. [13]
Растворимость жидкости при постоянном давлении приближенно описывается уравнением изобары растворимости (V.2), но с другими значениями коэффициентов А и В. [14]
На рис. 9.30, а, б, в приведены изобары растворимости водорода соответственно в железе, меди и алюминии. [15]
Страницы: 1 2 3 4