Восстановление - ион - водород
Cтраница 2
При этой реакции происходит восстановление иона водорода в газообразный водород. [16]
Как известно, реакция восстановления ионов водорода проходит на различных металлах при различных потенциалах. [17]
Наиболее часто встречаются реакции восстановления иона водорода до газообразного водорода и реакции ионизации кислорода с образованием ионов гидроксила. [18]
В общем виде кинетика восстановления ионов водорода рассмотрена в работах [6] и [8] с учетом доли поверхности, занятой адсорбированными атомами водорода. [19]
Реакции кислот могут сводиться к восстановлению ионов водорода, а также к окислению или восстановлению других частей молекулы. Мы обсудим восстановление протонов, которое более детально изучено в ацетонитриле и диметилсульфоксиде. [20]
Отсюда вытекает, что при восстановлении иона водорода на ртути, по-видимому, нет заметной зависимости коэффициента переноса заряда от потенциала в широком интервале потенциалов. Правда, по общему признанию, совпадение точек при - - 1 мксек пока не является полностью удовлетворительным. Однако не следует слишком критически рассматривать эти систематические ошибки, поскольку экспериментальные данные, полученные в самой верхней области потенциалов, служат главным образом для иллюстрации возможностей метода. Вероятно, впоследствии эти трудности в основном будут преодолены. [21]
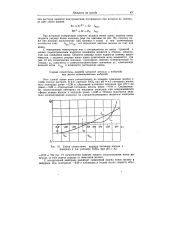 |
Схема совместного разряда катионов железа и 1водорода в 1-я. растворе РеЗСч при рН 4 5. [22] |
На рис. 19 схематически показан процесс восстановления ионов водорода за счет отдачи зарядов от окисления железа. [23]
В учебной литературе эти процессы описываются через восстановление ионов водорода и окисление ионов гидроксила, образуемых в результате диссоциации воды. Согласно новым воззрениям в этом случае происходит восстановление и окисление молекул воды. Следует учитывать, что вода образует лишь ничтожно малые количества Н и ОН - - ионов. [24]
МИЭ); в последнем случае исключается восстановление ионов водорода и растворенного кислорода. [25]
Существует несколько теорий, объясняющих различную скорость восстановления ионов водорода на разных металлах. Теории водородного перенапряжения исходят из представления о том, что при восстановлении ионов водорода имеется ряд последовательных стадий ( дегидратация, акт разряда, рекомбинация, возникновение пузырьков и др.), из-которых одна илн несколько являются замедленными. [26]
Поэтому Сг окисляется до Сг за счет восстановления ионов водорода. [27]
Если все волны деполяризатора расположены раньше волны восстановления ионов водорода, метод скрытых предельных токов водорода позволяет определить стехиометрию только суммарной реакции. [28]
Проверка уравнения (37.38) была проведена для реакции восстановления ионов водорода из раствора соляной кислоты. [29]
Во второй фазе катодной реакцией является реакция восстановления иона водорода, и этому периоду соответствует медленная стадия растворения олова. Скорость коррозии по своему значению в этот период соответствует коррозионному току порядка 10 - 9 А / см2 из-за недостатка эффективных катодов. Качество поверхности стали в порах, а также в царапинах или других нарушениях покрытия может оказывать определенное влияние на скорость коррозии. Небольшие размеры зерен оловянного покрытия также могут способствовать значительному увеличению скорости коррозии. [30]
Страницы: 1 2 3 4