Инициирование - окисление
Cтраница 2
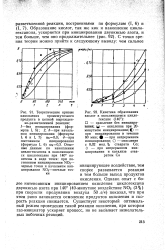 |
Теоретические кривые накопления промежуточного продукта в цепной вырожден.| Кинетика образования кислот в окисляющемся циклогексане ( 140. [16] |
Однако, опыт с более интенсивным инициированием окисления циклогексана двуокисью азота при 140 ( 40-минутное воздействие NO2 ( 3 %) при скорости продувания воздуха 50 л / ч) показал, что при этом рано начинается осмоление продуктов окисления и скорость реакции снижается. Существует некоторый оптимальный режим проведения такой реакции окисления, при котором газ-инициатор ускоряет процесс, но не вызывает нежелательных побочных реакций. [17]
Минимальная температура, необходимая для инициирования окисления, больше зависит от катализатора, чем от природы окисляемого [4] углеводорода. Выделяющееся тепло реакции быстро нагревает слой катализатора до более высокой температуры. Обычно реакция контролируется путем регулировки температуры охлаждающей бани таким образом, чтобы максимальная температура, измеряемая в слое катализатора, поддерживалась постоянно в нужном интервале. При температурах, значительно превышающих 600, происходит чрезмерное переокисление и реакцию становится трудно контролировать. [18]
Сопоставление этих данных с полученными при инициировании окисления окислами металлов ( рис. 3, а и б), свидетельствует о том, что к окисним катализаторам нужно подходить дифференцированно. Из рис. 3, а видно, что при катализе закисью никеля ( катализатор малоактивный в реакции разложения гидроперекиси [.]) зависимость скорости образования ацетофенона ( Т АФ)) и диметилфенилкарбинола О дмФк), образующихся из RO, от RH аналогична зависимости, полученной при гомогенном инициировании окисления кумола азо-бмс-изобутиро-иитрилом. Для окислов, катализирующих распад гидроперекиси ( например, AgO), зависимости скоростей образования АФ и ДМФК от [ RH ] ( рис. 3, б) отличаются от зависимостей, полученных при инициировании окисления кумола закисью никеля. [19]
Имея в виду применение фотохимических методов для инициирования окисления углеводородов и для изучения механизма этих реакций, мы провели работу по фотоинициированию реакции окисления 2 7-диметил-октана молекулярным кислородом. [20]
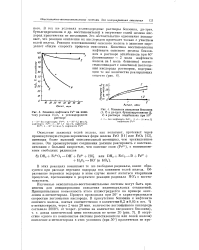 |
Кинетика окисления бензоина. [21] |
Изученные окислительно-восстановительные системы могут быть применены для инициирования окисления индивидуальных соединений. Принципиальная возможность этого иллюстрируется на примере окисления а-метилстирола. [22]
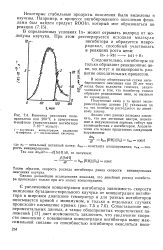 |
Кинетика окисления полипропилена пои 200 С в присутствии а-нафтола ( концентрация ингибитора 7 - 10 5 моль / г. [23] |
Таким образом, скорость расхода ингибитора равна скорости инициирования окисления каучука. [24]
Эта оценка, несомненно, является завышенной, так как возможно инициирование окисления также за счет реакций соли двухвалентного железа и радикала СавНзвСЬ, а реакции этих частиц не учитывались при подсчете длины цепи. [25]
По окончании индукционного периода взаимодействие масла с кислородом быстро развивается, начинается процесс инициирования окисления. Он сопровождается выделением тепла и интенсивным образованием первичных продуктов окисления - гид-ропероксидов. [26]
Таким образом, скорость расхода Ф - - НА равна или пропорциональна скорости инициирования окисления. [27]
Таким образом, скорость расхода Ф - - НА равна или пропор циональна скорости инициирования окисления. [28]
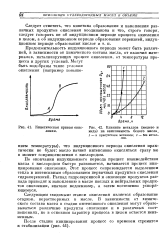 |
Влияние металлов ( железо и медь на окисляемость белого масла. 1 - в присутствии металлов. 2 - без металлов. [29] |
По окончании индукционного периода процесс взаимодействия масла с кислородом быстро развивается, начинается процесс инициирования окисления. Этот процесс сопровождается выделением тепла и интенсивным образованием первичных продуктов окисления гидроперекисей. Распад гидроперекисей и окисление продуктов распада приводят к накоплению в масле кислых и нейтральных продуктов окисления, вначале медленному, а затем постепенно ускоряющемуся. [30]
Страницы: 1 2 3 4