Аква-комплекс
Cтраница 1
Окраска аква-комплексов катионов, имеющих незаполненные d - орбитали, обусловлена возможностью легких переходов между энергетически близкими d - орбиталями. [1]
Окраска аква-комплексов катионов, имеющих незаполненные d - орбитали, обусловлена возможностью легких переходов между энергетически близкими с ( - орбиталями. [2]
Вокруг самого аква-комплекса имеется гидратная оболочка со слаСыми Связями, затрата энергии на ее диссоциацию также входит в общий баланс, который по величине равен обратному процессу - гидратации иона. Аналогично, нейтрализация иона Мп противоположна процессу ионизации, а образование кристалла - сублимации. Таким образом, нормальный электродный потенциал может быть связан с энергиями гидратации ( гл. При этом следует иметь в виду, что эти величины представляют собой изменение ДЯ0, поэтому для перехода к энергии Гиббса необходимо учесть изменение энтропии. [3]
Более устойчивыми, чем аква-комплексы меди, являются ам-мин-комплексы. Они легко образуются при действии аммиака на соли меди. [4]
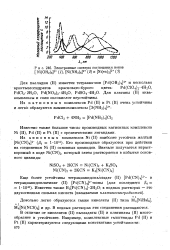 |
Электронные спектры поглощения ионов [ Ni ( OH2 6p ( I, [ Ni ( NH3 6p ( 2 и [ № ( еп з ] 2 ( 3. [5] |
Для платины ( II) аква-комплексы и соли оксокислот неустойчивы. [6]
Спирт действует дегидратирующим образом на аква-комплекс кобальта, последний в присутствии спирта теряет две молекулы воды, при этом координационное число кобальта не меняется. [7]
Процессы переноса электронов между аквакомплексами или аква-комплексом и комплексом, содержащим наряду с лигандами координированные молекулы воды, характеризуются близкими значениями свободной энергии и энтропии активации. [8]
Из катионных комплексов для Со ( II) наиболее характерны аква-комплексы [ Со ( ОН2) 6 ] 2, придающие растворам ярко-розовую окраску. [9]
Некоторые из них не численные, потому что в таких случаях образовавшиеся аква-комплексы перегруппировываются со скоростями, сравнимыми со скоростями их образования, и удовлетворительный количественный анализ таких налагающихся реакций еще не сделан. [10]
Чтобы иметь универсальный критерий сравнения, пользуются стандартными электродными потенциаламн ионов аква-комплексов. [11]
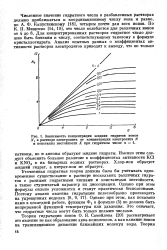 |
Зависимость концентрации жидких гидратов ионов. [12] |
Теория гидратации ионов О. Я. Самойлова [20] рассматривает это явление не как образование аква-комплексов, а как влияние ионов на трансляционное движение ближайших молекул воды. [13]
Чтобы иметь универсальный критерий сравнения, пользуются стандартными электродными потенциаламн ионов аква-комплексов. [14]
Полный перенос кислорода происходит при восстановлении гидроксо-комплексов и по крайней мере 60 % при восстановлении исходного аква-комплекса. [15]
Страницы: 1 2 3