Активность - ион - натрий
Cтраница 2
Коэффициент риЛ7а1 / Л а2 показывает отношение числа мест с разной активностью; аи равно отношению коэффициентов активности ионов натрия к активности иона водорода. [16]
Таким образом, потенциал стеклянного электрода является функцией не только активности ионов водорода в растворе, но и функцией активности ионов натрия в растворе. [17]
Таким образом, потенциал стеклянного электрода является функцией не только активности ионов водорода в растворе, но и функцией активности ионов натрия в растворе. [18]
Таким образом, потенциал стеклянного электрода является функцией не только активности ионов водорода в растворе, но и функцией активности ионов натрия в растворе. [19]
В то же время возможна ранняя диагностика засоления почв по электрической проводимости почвенного раствора, осолонцевания - по рН и активности ионов натрия, загрязнения тяжелыми метдл-лами - по показателям ферментативной активности почвы. [20]
Чтобы по возможности строго судить, соответствуют ли изменения потенциала стеклянного электрода функции натриевых электродов, были приняты во внимание изменения коэффициентов активности ионов натрия - в растворах. Значения последних принимались численно равными средним коэффициентам активности электролитов, в которые входят ионы натрия. Расчеты показали, что зависимость потенциала стеклянного электрода от логарифма активности ионов натрия в растворе приближается к линейной. Однако рассмотренная выше нормировка коэффициентов активности ионов была принята произвольно, а поэтому доказательство натриевой функции стеклянных электродов, данное в этой работе, не может считаться термодинамически строгим. [21]
Чтобы по возможности строго судить, соответствуют ли изменения потенциала стеклянного электрода функции натриевых электродов, были приняты во внимание изменения коэффициентов активности ионов натрия в растворах. Значения последних принимались численно равными средним коэффициентам активности электролитов, в которые входят ионы натрия. Расчеты показали, что зависимость потенциала стеклянного электрода от логарифма активности ионов натрия в растворе приближается к линейной. Однако рассмотренная выше нормировка коэффициентов активности ионов была принята произвольно, а поэтому доказательство натриевой функции стеклянных электродов, данное в этой работе, не может считаться термодинамически строгим. [22]
Интересно отметить, что активность ионов натрия в растворах NaCl и NaNO3 в результате магнитной обработки несколько повышается, в то время как активность ионов водорода всегда понижается. Причиной повышения активности ионов натрия, по-видимому, является то, что гидратация их становится отрицательной. [23]
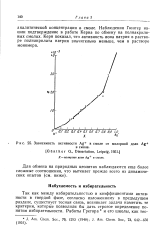 |
Зависимость активности Ag в смоле от молярной доли Ag. [24] |
Керн показал, что активность иона натрия в растворе полиакрилата натрия значительно меньше, чем в растворе мономера. [25]
В отсутствие солей изменение как коэффициента активности ионов натрия ( определенного с помощью мембранного электрода), так и удельной электропроводности характеризовалось двумя скачками ( примерно 2 - 10 - 4 и 4 - 10 - 4 Мг. [26]
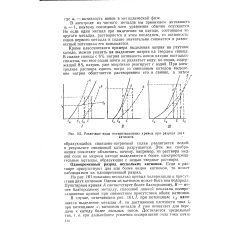 |
Различные виды поляризационных кривых при разряде двух. [27] |
В сплаве свинца с 6 % натрия активность ионов натрия настолько снижена, что этот сплав почти не разлагает воду; но сплав, содержащий 8 % натрия, уже энергично реагирует с водой. [28]
Однако этим не исчерпываются затруднения при определении активности отдельных ионов. Допустим, мы бы нашли способ определения коэффициентов активности ионов натрия отдельно, но и это не привело бы к цели, так как активность иона натрия зависит от активности анионов - при той же концентрации активность иона натрия в присутствии ионов хлора будет иной, чем в Присутствии сульфат-ионов. [29]
Вывод, который был только что сделан, основан на предположении, что в пленке стекла активность ионов водорода не зависит от активности ионов натрия и наоборот. [30]
Страницы: 1 2 3