Активность - катион
Cтраница 3
Отсюда следует, что потенциал амальгамного электрода зависит от активности катиона в растворе, а также от активности компонента в металлической фазе. [31]
Отсюда следует, что потенциал амальгамного электрода зависит от активности катиона в растворе и активности компонента в металлической фазе. [32]
Электроды 3-го рода изменяют свой потенциал в зависимости от активности катионов чужеродного металла. [33]
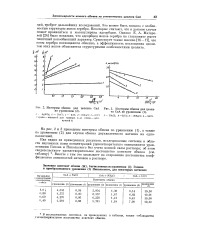 |
Изотермы обмена для цеолита СаА по уравнению ( 2.| Изотермы обмена для цеолита СаА по уравнению ( 1.. T - NAC1. 2 - КС1. 3 - NH. C1. 4 - L1C1. [34] |
Вместе с тем это указывает на сохранение постоянства коэффициентов активностей катионов в растворе. [35]
Так, изученные катализаторы располагаются в следующем порядке по убывающей активности катионов: Cd ZnSrBaCaMgMn CuAlPbHg. Соли же никеля оказывают нежелательное влияние. [36]
Хотя мембранные электроды применялись с большим успехом для измерения активностей катионов главной подгруппы 1 - й и 2 - й групп, они имеют ряд специфичных недостатков. Вообще говоря, надежные измерения в значительной степени ограничиваются растворами, которые содержат только один катион, и в этих случаях не нужно использовать постоянную ионную среду для контроля коэффициентов активности. Однако, по-видимому, возможно разработать селективные мембраны, проницаемые для одних катионов и непроницаемые для других. Например, потенциал электрода из калийной глины ( potassium clay) не зависит от концентрации ионов кальция, и предполагается [87], что растворы, содержащие пары катионов, можно будет исследовать с применением двух мембран с разной проницаемостью для двух ионов. Грегор и Схонхорн [86] сообщили, что многослойный стеарат бария с осью ориентации, перпендикулярной направлению переноса, обратим к ионам бария в присутствии ионов натрия. Равновесие достигается быстрю, но так как электрод обладает большим сопротивлением, необходимо использовать ламповый потенциометр. [37]
В щелочных лее растворах потенциал электрода в основном определяется активностью катионов щелочных металлов и, следовательно, его можно использовать для определения активности соответствующего катиона. [38]
Она равна аКакаа, где а, и аа - активности катиона и аниона. [39]
 |
Ячейка для измерения диффузионных потенциалов концентрационной цепи. [40] |
Для исследования были выбраны растворы хлорида калия, в которых активности катионов и анионов близки. [41]
По измерениям компенсирующих напряжений соответствующих вольта-цепей независимо находили реальные коэффициенты активности катиона ( у) и аниона ( vl), входящих в состав данного электролита. [42]
Электродами первого рода называют такие, электродный потенциал которых определяется активностью катионов, одноименных с металлом, погруженным в электролит. Типичный электрод первого рода состоит из пластинки металла, погруженного в раствор его соли или в расплавленную соль этого металла. [43]
Различают электроды, обратимые относительно катиона ( потенциал электрода зависит от активности катионов в растворе) и обратимые относительно аниона. Примером первых может служить цинковый и медный электроды в растворах их солей. [44]
Средний коэффициент активности электролита Y представляет собой среднее геометрическое из коэффициентов активности катиона и аниона, а средняя концентрация ионов электролита т - среднее геометрическое из концентраций катиона и аниона. [45]
Страницы: 1 2 3 4