Активность - комплекс
Cтраница 1
Активность комплексов ( МС1Ж - 4С3Н6О) убывает в ряду Fe Al Sn Ti. Различие в поведении хлоридов авторы объясняют различием механизмов полимеризации: координационно-катионного в первом случае и координационного во втором. При этом энергия активации полимеризации по второму механизму значительно более высока. [1]
Активность комплекса ( РеОН) адс найдем из записи реакций ( 1) и ( 2), участники которых находятся в равновесии. [2]
Активность комплекса катализатор - сокатализатор зависит от его способности отдавать протон. Так, было установлено, что скорость полимеризации изобутилена с SnQ4 в качестве катализатора возрастает с увеличением кислотности сокатализатора. Скорость уменьшается в ряду: уксусная кислота нитроэтан фенол вода. В большинстве случаев максимальной скорости полимеризации соответствует некоторое определенное отношение сокатализатора к катализатору. Выше и ниже этого оптимального значения отношения сокаталпза-тор / катализатор скорость полимеризации уменьшается. [3]
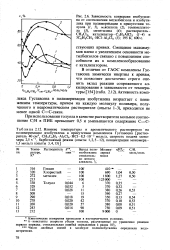
Активность комплекса Густавсона в полимеризации изобутилена возрастает с понижением температуры, причем на каждую молекулу полимера, полученного в неароматическом растворителе ( опыты 1 - 3), приходится не менее одной ОС-связи. При использовании толуола в качестве растворителя мольное соотношение С / Н в ПИБ превышает 0 5 и уменьшается содержание ОС-связей, молекулярная масса и выход полимеров ( опыты 5 - 12), что связано с образованием алкилароматичес-ких соединений. Выше 273 К полимеризация изобутилена в толуоле вырождается в реакцию алкилирования арена мономером с образованием легкого алки-лата с т.кип. до 523 К / 98 кПа, состоящего на 31 6 % из м - и 43 4 % п-трет-бутил-толуолов ( мол. [4]
 |
Зависимость каталазной активности комплексных соединений. меди от природы лигандов. [5] |
Активность белково-биуретовых комплексов хотя и слабо, но все же зависит и от природы белка. Глобулины дают наиболее активные комплексы, затем следует желатин, казеин и альбумины. Так как размах каталазной активности, свойственной различным комплексам меди, очень велик, то естественны попытки найти последовательность, в которой изменяется активность, располагая в ряд не индивидуальные лиганды, а группы комплексов, образованных лигандами, относящимися к одному классу органических соединений. Действительно, групповые характеристики показывают, что внутри группы сходных лигандов активность изменяется в некотором интервале, причем, насколько можно судить по-имеющимся данным, чем выше общий уровень активности, тем в общем шире интервал, занимаемый данной группой. [6]
Активность комплекса Густавсона в полимеризации изобутилена возрастает с понижением температуры, причем на каждую молекулу полимера, полученного в неароматическом растворителе ( опыты 1 - 3), приходится не менее одной СС-связи. [8]
Аналогично изменяется активность комплексов СиЦХ в Реакции распада гидропероксидаы-фенилэтила. Скорость распада гидро-пероксида существенно зависит также от природа растворителя. [9]
Резкое снижение активности комплекса при замене одного алкила в А1 ( С2Н5) з на хлор, вероятно, связано с повышением электроноакцепторных свойств этого АОС. В еще большей мере этот эффект проявляется в дизамещенном этилалюминийдихлориде, скорость полимеризации в присутствии которого ничтожно мала. Замена одной этильной группы в Al ( C2Hsb на водород увеличивает электронодонорные свойства АОС. Соответственно повышается активность в полимеризации каталитического комплекса с этим соединением. По-видимому, связь Ti - С в этом комплексе обладает оптимальной лабильностью. [10]
Сопоставление результатов активности комплекса ФГ в групповой ситуации с данными, полученными у больных гипертонической болезнью в условиях эмоционального напряжения первой модели, показало большую лизирующую активность комплекса в конфликтной ситуации, что, очевидно, свидетельствует о большой степени эмоционального напряжения в этой модели, что находит свое подтверждение и в том факте, что в этой модели эмоционального напряжения только у одного больного не произошло активации комплекса ФГ, тогда как в первой модели у 16 больных литическая активность комплекса ФГ отсутствовала и после эмоционального напряжения. Последнее позволяет нам утверждать, что у этой части больных реакция ВПС на эмоциональное напряжение сохранена, а отсутствие этой реакции в индивидуальной ситуации, вероятно, обусловлено сниженной мотивацией больных в данной ситуации. [11]
Оказалось, что активность комплекса ФГ в условиях группового взаимодействия была самой высокой ( 73 5 5 62 мм2) у больных 1 - й группы, для которых были характерны реакции конфликтного типа, сопровождающиеся неадекватными поведенческими компонентами - взаимными обвинениями, речевой расторможен-ностью, повышенной моторной активностью, ухудшением навыка. [12]
Различия в повышении активности комплекса ФГ по сравнению с лицами контрольной группы обнаружены нами в первой группе больных, у которых уровень лизирующей активности комплекса ФГ перед эмоциональной нагрузкой оказался одинаковым. [13]
 |
Зависимость активности комплекса от структуры адденда. [14] |
Важнейшим фактором, определяющим активность комплекса, является природа адденда. [15]
Страницы: 1 2 3 4