Активность - пар
Cтраница 2
В случае выполнимости закона Генри существует линейное соотношение между концентрацией и давлением ( или активностью пара), при этом 5 постоянно. [16]
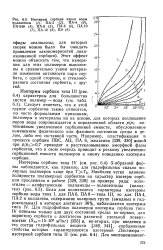 |
Изотермы сорбции паров воды коллагеном ( Л, ПА-2 ( 2, ПА-4 ( 3, 28 ПА-548 ( 4, ПА-6 ( 5, ПА-8 ( 6, ПА-10 ( 7, ПА-12 ( 8, ПЭ ( 9. [17] |
Этот эффект можно объяснить тем, что измерения для этих полимеров выполнены в сравнительно узком интервале изменения активности пара сор-бата, с одной стороны, и стеклообразного состояния сорбента, с другой. [18]
 |
Концентрационная зависимость. [19] |
Принято считать, что наиболее показательной для систем полимер - вода является зависимость коэффициента взаимодиффузии от количества сорбированной влаги или активности пара. [20]
Для иприр и Ри239 при уменьшении их концентрации ( активности) в 1000 раз ( U-001 %), a La140 в 15 раз ( 0 33 мкюри / л) активность пара будет отвечать ПДК - Но для Ри239 превышение дозы в паре столь велико, что 1 л пара может довести до ПДК тысячи кубических метров воздуха и, значит, может сделать опасным пребывание в комнате самого большого размера. Ожидаемая большая активность водяного пара плутониевых и урановых растворов заставляет нас принять, что вне мощной тяги кипячение их недопустимо. [21]
Исследование перехода в пар радиоактивных нелетучих по обычным представлениям веществ при выпаривании растворов показало, что механизм захвата здесь сводится к уносу паром мельчайших капель раствора. Активность пара при этом составляет тысячные, десятитысячные и даже меньшие доли ( от активности исходного раствора) в зависимости от скорости кипения, высоты дефлегматора и других факторов. [22]
Метод точки кипения основан на том, что скорость испарения вещества при достижении точки кипения существенно изменяется. Поэтому кривая, выражающая зависимость активности пара от времени, будет характеризоваться изломом, отвечающим температуре кипения. Поскольку температура кипения соответствует насыщенному пару, анализ кривой активность пара - время позволяет определить давление насыщенного пара. [23]
В первом варианте для измерения давления пара исследуемое вещество помещают в замкнутое пространство с постоянной температурой, в котором предварительно создается высокий вакуум. Таким методом легко измерить изменение активности пара в зависимости от температуры и найти теплоту испарения в измеренном интервале температур. Для перехода к абсолютным значенлям давления пара необходимо знать его при одной из температур или найти коэффициент перехода от измеренной активности к абсолютной. Для этого целесообразно калибровать прибор с помощью вещества с известной удельной активностью, содержащего данный изотоп. [24]
Метод точки кипения основан на том, что скорость испарения вещества при достижении точки кипения существенно изменяется. Поэтому кривая, выражающая зависимость активности пара от времени, будет характеризоваться изломом, отвечающим температуре кипения. Поскольку температура кипения соответствует насыщенному пару, анализ кривой активность пара - время позволяет определить давление насыщенного пара. [25]
Для любой системы типа паров углеводорода в полиэтилене коэффициент растворимости Я не постоянен, а увеличивается с ростом концентрации проникающего вещества, как и D. Проницаемость быстро увеличивается с возрастанием парциального давления или активности пара. [26]
Ампулу подготавливают к работе, помещают в печь и определяют активности паров / п при желаемых температурах. При каждой температуре ампулу выдерживают до тех пор, пока активность пара не станет постоянной. [27]
В этой таблице приведено суммарное, по сравнению с исходной системой, уменьшение активности продукта превращения, так называемый коэффициент очистки. Эта величина показывает, например, во сколько раз вся активность пара меньше активности исходного раствора. [28]
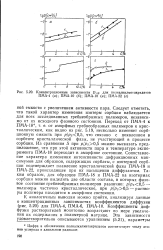 |
Концентрационные зависимости DI ф для полиалкилметакрилатов ПМА-4 ( а. ПМА-10 ( б. ПМА-18 ( а. ПМА-22 ( г. [29] |
Следует отметить, что такой характер изменения изотерм сорбции наблюдается для всех исследованных гребнеобразных полимеров, независимо от их исходного фазового состояния. Из сравнения S при p / ps0 5 можно высказать предположение, что при этой активности пара и температуре эксперимента ПМА-18 переходит в аморфное состояние. Сопоставление характера изменения интенсивности дифракционных максимумов для образцов, содержащих сорбаты, с изотермой сорбции подтверждает плавление кристаллической фазы ПМА-18 и ПМА-22, происходящее при их насыщении диффузантом. Таким образом, для образцов ПМА-18 и ПМА-22 на изотермах сорбции можно выделить две области состава, в которых фазовое состояние гребнеобразных полимеров различно: p / ps0 5 - полимеры частично кристаллические, при p / / os0 5 - - растворы полимера находятся в аморфном состоянии. [30]
Страницы: 1 2 3