Активность - первое
Cтраница 1
Активность первого должна составлять около 1000 имп. Смесь накапывают на фильтр и фильтр подсушивают. [1]
Отношение коэффициентов активности первого и второго компонентов в зависимости от х при х3 0 выражается кривой 2 ( как и на рис. VI. При этом наиболее простые соотношения имеют место, если линия / - прямая. [2]
Осадок отфильтровывают и измеряют активности первого и второго осадков. [3]
Однако при температуре около 320 активности первого и последнего членов этого ряда близки по значению, а выше - 320 -меняются местами. [4]
Однако при температуре около 320 активности первого и последнего членов этого ряда близки по значению, а выше 320 -меняются местами. [5]
Как в кислом, так и в щелочном растворе активность первого оказывается намного выше. В наблюдается прямая реакция до воды. [6]
Сопоставление катализаторов СВД и БАВ показывает, что при температуре 485 С активность первого меньше, чем второго, что, очевидно, обусловлено менее выгодной структурой диатомита - носителя СВД. [7]
Таким образом, если сопоставить наиболее эффективный бис-фенол с наиболее эффективным моноалкилфенолом, то при использовании их в смесях с фосфонатом противоокислительная активность первого в 10 раз превышает активность второго. [8]
Заметим, кстати, что константы А и В в этих уравнениях имеют ясный физический смысл: они выражают значения коэффициентов активности первого ( константа А) и второго ( константа В) компонентов при их бесконечно малой концентрации в растворах. [9]
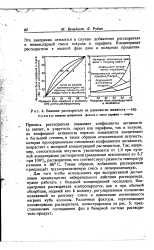 |
Влияние растворителя на равновесие жидкость - пар. Пример. влияние добавления фенола к смеси парафин - толуол. [10] |
Примесь растворителя повышает коэфициенты активности ( а значит, и упругость паров) как парафина, так и толуола, но коэфициент активности первого повышается значительно в большей степени, и таким образом относительная летучесть, которая пропорциональна отношению коэфициентов активности, возрастает с молярной концентрацией растворителя. Так, например, относительная летучесть увеличивается от 1 0 при нулевой концентрации растворителя ( разделение невозможно) до 3 7 при Ю0 / 0 растворителя, что соответствует разности температур кипения в 36 С. Таким образом, добавление растворителя превращает трудноразделяемую смесь в легкоразделимую. [11]
Независимо от того, справедливо ли для данной системы правило Харнеда или нет, при постоянной моляльной концентрации в растворах электролитов одинакового типа добавка к данному электролиту второго, имеющего более высокий коэффициент активности, повышает коэффициент активности первого, и наоборот. Однако коэффициент активности первого электролита, как правило, не повышается до значения, равного коэффициенту активности второго, и при бесконечном разбавлении на фоне второго остается несколько ниже последнего. [12]
Пусть в растворе содержится а ммолей одного из ионов исследуемого соединения. Осадок отфильтровывают и измеряют активность первого ( / t) и второго ( / 2) осадков. Если эффективная растворимость соединения составляет к ммолей / мл, то в растворе после первого осаждения останется xV1 ммоля, следовательно, в осадок перешло а-xVi ммоля. [13]
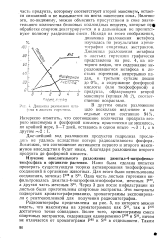 |
Динамика разложения метафоса в листьях гортензии. [14] |
Возможно, что соотношение активности первого и второго максимумов впоследствии будет иным, благодаря разложению второго продукта до фосфорной кислоты. [15]
Страницы: 1 2