Активность - платина
Cтраница 1
Активность платины превышает на два порядка активность золота и в 40 раз активность палладия. [1]
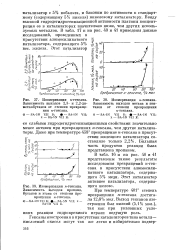
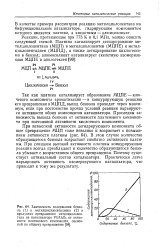
Ввиду высокой гидродегидрогенизационной активности платины концентрация ее в катализаторах значительно ниже, чем других используемых металлов. В табл. 17 и на рис. 40 и 41 приведены данные исследований проведенных в присутствии алюмосиликатного § катализатора, содержащего 5 % § вес. [3]
Для постепенного подавления активности платины в промежутках между последовательными испытаниями в поток водорода, проходящий через катализатор, вводились порции по / 64 см3 ( НТД) газообразного сероводорода. [4]
Стоит напомнить, что активности платины и палладия в реакции конфигурационной изомеризации диалкилцикланов ( см. выше) располагаются в противоположной последовательности. [5]
Таким образом, факт снижения активности платины в кислородной реакции при ее раздроблении до размеров менее 15 А на углеродном носителе является весьма достоверным. Эффект ускорения водородной реакции при переходе к очень мелким частицам платины менее достоверен, так как не подтверждается результатами работ на высокодисперсных углеродных носителях. Возможно, однако, дальнейшие исследования устранят это противоречие, когда более глубоко будет понято влияние типа углеродного носителя на электронные свойства промотора. [6]
 |
Изменение активности платинового контакта. [7] |
На этом уровне ( отрезок ab) активность платины удерживалась в течение нескольких часов и в отсутствие электрического заряда на катализаторе. [8]
В этом случае количество образующегося бензола возрастает симбатно активности платины. При слишком высокой активности платины конкурирующая реакция всегда преобладает и количество образующегося бензола убывает с возрастанием общего превращения. Поэтому существует оптимальный состав катализатора. Практически легче варьировать активность изомеризующего катализатора, что приводит к тому же результату. [10]
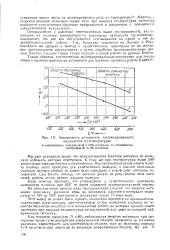 |
Зависимость активности платинированного. [11] |
Надо поэтому признать, что утверждение о существовании максимума активности платины при 525 не имеет надежной экспериментальной основы. [12]
Обнаруженные на ранних стадиях исследования примеры отравления относятся главным образом к активности платины в реакции окисления и сходных реакциях ( превращение двуокиси серы в трехокись, реакция образования воды из гремучего газа, разложение перекиси водорода), но основное применение эта группа металлов находит, пожалуй, в реакциях гидрирования. Действительно, большинство из современных работ по отравлению было проведено в связи с этим типом реакций. Металлы вертикальной группы: никель, палладий и платина, особенно важны благодаря их высокой общей активности и вследствие широкого применения их как для гидрирования, так и для дегидрирования. Меньшая активность кобальта и особенно меди сообщает этим элементам особые свойства, которые иногда полезны. Так, наиболее мягкое действие меди как катализатора гидрирования часто допускает выделение промежуточных продуктов, а применение меди вместо никеля для дегидрирования при высоких температурах обычно приводит к меньшему образованию продуктов разложения; далее, кобальт ( подобно никелю и, в меньшей степени, железу) является эффективным катализатором в специальном случае синтеза жидких углеводородов путем конденсационной гидрогенизации окиси углерода по методу Фишера-Тропша. Основное использование железо находит, однако, в синтезе аммиака, представляющем реакцию, близкую к гидрированию. Все эти процессы очень чувствительны к отравлению. Серебро и золото имеют незначительную активность для обычного гидрирования и поэтому в табл. 1 поставлены в скобки; однако они использовались как эффективные катализаторы в особом случае восстановления нитробензола водородом до анилина [1], при окислительном дегидрировании метилового спирта до формальдегида. [13]
В литературе первые упоминания об отравлении платины сернистыми соединениями относятся главным образом к активности платины в реакции окисления и сходных реакциях. Так, Шенбейн в 1843 г. наблюдал, что платиновая спираль или чернь, введенные на мгновение в атмосферу H2S, теряют свою активность по отношению к гремучей смеси. [14]
К недостаткам этого метода следует отнести то, что образующаяся при сожжении двуокись кремния снижает активность платины, оседая на ее поверхности. Необходимое охлаждение трубки перед взвешиванием значительно удлиняет время анализа, взвешивание сравнительно большой по длине трубки для сожжения на аналитических весах громоздко и приводит к ошибкам. Очевидно, указанные недостатки послужили причиной ограниченного использования метода. [15]
Страницы: 1 2 3 4