Каталитическая активность - окись - алюминий
Cтраница 1
Каталитическая активность окиси алюминия существенно зависит также от наличия на ее поверхности воды, щелочей, галогенов и минеральных кислот. Нанесение на окись алюминия КОН ( или NaOH) приводит к большей селективности образования цис-бутена-2 из бутена-1. [1]
Каталитическая активность окиси алюминия, обработанной соляной кислотой, обусловлена главным образом наличием на ее поверхности химически связанного хлора. Как уже отмечалось, последний может появиться только в результате взаимодействия поверхностных гидроксильных групп с НО. Однако не каждый поглощенный ион хлора способствует появлению активного центра. Атомы алюминия в окиси алюминия в зависимости от своего положения в кристаллической решетке могут быть связаны с одной или с двумя гидроксильными группами. Мы считаем, что окись алюминия приобретает каталитические свойства только в том случае, когда ионом хлора замещается одна из парных гидроксильных групп, причем атом водорода другой гидроксильной группы благодаря соседству электроотрицательного хлора становится подвижным и способным к диссоциации с образованием протона. [2]
 |
ИК-спектры гидроксофтори дов алюминия в зависимости от содержания фтора и условий обработки. [3] |
Для выяснения природы каталитической активности фторированной окиси алюминия, гидроксофторидов и их смеси с фтористым алюминием было проведено комплексное исследование их свойств. В работе были использованы методы рентгеноструктурного, адсорбционного, термографического и кинетического анализов, ИКС и ЯМР, различные методы определения поверхностной кислотности. [4]
Влияние фтористого бора на каталитическую активность окиси алюминия и алюмосиликатов. [5]
Влияние фтористого бора на каталитическую активность окиси алюминия и алюмосиликатов для реакции крекинга кумола и дегидратации этилового спирта. [6]
В табл. 14 приведены результаты испытаний каталитической активности окиси алюминия с различным содержанием хлора. [7]
Длительный период эксплуатации катализаторов приводит к уменьшению поверхности и каталитической активности окиси алюминия. Однако наиболее значительные изменения обусловлены укрупнением мелких кристаллитов, в результате которого снижается удельная активность платины и уменьшаются гидро - и дегидрогенизационные функции катализаторов. Изменения, вызывающие снижение дегидрирующей активности катализатора, происходят наиболее быстро; в результате реакции дегидрирования подавляются и преобладают реакции кислотного катализа. В конечном итоге усиливается процесс коксообразования, уменьшаются выходы бензинов и увеличиваются выходы газов. Чем в более жестких условиях проводится процесс, тем отчетливее проявляется тенденция кристаллитов платины к укрупнению. [8]
Фегем и Сваллоу [9] показали, что уменьшение содержания натрия увеличивает каталитическую активность окиси алюминия в реакции дегидратации этанола до этилена. [9]
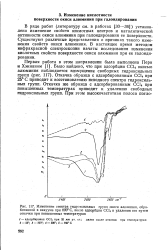 |
Изменение спектра гидроксильных групп окиси алюминия, обработанной в вакууме при 800 С, после адсорбции СС14 и удаления его путем откачки при повышенных температурах. [10] |
В ряде работ ( литературу см. в работах [30-36]) установлено изменение свойств кислотных центров и каталитической активности окиси алюминия при галоидировании ее поверхности. Существуют различные представления о причинах такого изменения свойств окиси алюминия. В настоящее время методом инфракрасной спектроскопии начаты исследования изменения кислотных свойств поверхности окиси алюминия при ее галоидировании. [11]
 |
Изомеризация н-бутенов в присутствии модифицированной окиси алюминия. [12] |
Окись алюминия является стабильным катализатором - в отличие от алюмосиликата и фторированной окиси алюминия она слабо катализирует реакции крекинга и полимеризации и не дезактивируется за счет этих процессов. Каталитическая активность окиси алюминия связана с ее строением. [13]
Однако большинство работ с окисью алюминия было предпринято с целью выяснения природы каталитически активных центров в дегидратированной окиси алюминия. Каталитическая активность окиси алюминия возрастает при обработке фтористоводородной кислотой. Вебб [ 3391 исследовал влияние обработки HF на адсорбцию NH3 окисью алюминия, причем никаких различий в адсорбционной емкости обнаружено не было. [14]
Имеются указания27, что кристаллы горного хрусталя обладают более высокой каталитической активностью, чем осажденная двуокись кремния. Каталитическая активность окиси алюминия лишь немного превосходит активность кремнезема. [15]
Страницы: 1 2