Каталитическая активность - поверхность
Cтраница 1
Каталитическая активность поверхности зависит от образования поверхностных связей с реагентами, промежуточных соединений и продуктов реакции, а также от скорости образования и разрыва этих связей. Поэтому существует взаимосвязь между скоростью поверхностной химической реакции и устойчивостью поверхностного соединения или самого устойчивого интерме-диата. [1]
Каталитическая активность поверхностей нередко, впрочем, в сильнейшей степени зависит от природы молекул. Молекулярная архитектура активных участков, несомненно, является чрезвычайно важным фактором в катализе. Пусть, например, молекула АВ адсорбируется на поверхности, период атомной решетки которой превышает нормальное расстояние АВ. Тогда при адсорбции молекула будет растягиваться и, вероятно, приближаться к реактивному состоянию. [2]
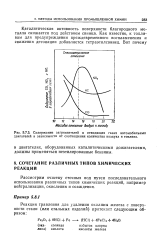 |
Содержание загрязнителей в отходящих газах автомобильных двигателей в зависимости от соотношения количества воздуха и топлива. [3] |
Каталитическая активность поверхности благородного металла снижается под действием свинца. Как известно, к топли-вам для предупреждения преждевременного воспламенения и снижения детонации добавляется тетраэтилсвинец. [4]
Если каталитическая активность поверхности велика, вполне возможно, что скорость реакции будет определяться скоростью процесса диффузии к поверхности катализатора или от нее. Такое положение часто преобладает в каталитических реакторах ( см. гл. Однако весьма часто скорость каталитической реакции определяется скоростями процессов десорбции ( для удобства можно считать, что десорбция означает процесс, объединяющий стадии 3 и 4) или адсорбции. Поэтому целесообразно ознакомиться с теоретическими способами определения скоростей этих процессов. Несомненно, одним из наиболее удачных методов определения скоростей адсорбции и десорбции следует считать способ, основанный на теории абсолютных скоростей реакций [63], которая вводит концепцию химического равновесия в область кинетики реакции с помощью методов статистической механики. [5]
Отсюда следует, что каталитическая активность поверхности по отношению к данной реакции определяется, с одной стороны, положением в энергетическом спектре локальных уровней всех участвующих в реакции частиц, или, иначе говоря, энергетическим спектром поверхности; с другой - положением уровня Ферми в этом энергетическом спектре. [6]
Даже в отсутствие примесей каталитическая активность поверхности металла может нарушаться водородным ядом. Под этим подразумевается уничтожение активных центров на поверхности металла реакцией рекомбинации атомов водорода. Поскольку каталитическое действие поверхности металла связано с дефектами кристалла, активные центры находятся в более высоких энергетических состояниях, ( чем поверхность идеального кристалла. За счет большой энергии, выделяемой при слиянии - атомов водорода, активные центры могут перейти в состояние с пониженной энергией ( поверхность идеального кристалла) и потерять свою каталитическую активность. Перед употреблением старого или долго проработавшего водородного электрода его следует повторно активировать или платинировать. [7]
Даже в отсутствие примесей каталитическая активность поверхности металла может нарушаться водородным ядом. Под этим подразумевается уничтожение активных центров на поверхности металла реакцией рекомбинации атомов водорода. Поскольку каталитическое действие поверхности металла связано с дефектами кристалла, активные центры находятся в более высоких энергетических состояниях, чем поверхность идеального кристалла. За счет большой энергии, выделяемой при слиянии атомов водорода, активные центры могут перейти в состояние с пониженной энергией ( поверхность идеального кристалла) и потерять свою каталитическую активность. Перед употреблением старого или долго проработавшего водородного электрода его следует повторно активировать или платинировать. [8]
Было показано, что каталитическая активность поверхности силикагеля, метоксилированной на 50 %, в отношении разложения муравьиной кислоты пренебрежимо мала. Это позволяет предположить, что только часть поверхностных ОН-групП является центрами, на которых протекает дегидратация. В исследованном интервале температур дегидратация протекает на протонных центрах поверхности, в то время как дегидрирование идет через поверхностные формиатные ионы. [9]
Однако есть основание полагать, что каталитическая активность поверхности железа в реакциях (1.4) и (1.5) будет уменьшаться при насыщении поверхности водородом. Это предположение основано на найденном А. [10]
Стиси и Элькин [423], сравнивая каталитическую активность поверхностей жидкого и твердого цинка, служащего катализатором при разложении метанола, указывают, что если указанная выше точка зрения верна, то плавление катализатора должно снижать его активность. [11]
В начале статьи было отмечено, что каталитическая активность поверхности определяется, с точки зрения электронной теории, двумя факторами: характером ее энергетического спектра, и, при заданном энергетическом спектре, положением в нем уровня Ферми. [12]
Полученные граничные условия показывают, что коэффициенты каталитической активности поверхности kwo и kw - в общем случае являются функциями не только температуры, давления и химического состава, но и диффузионных потоков компонентов. В [117] исследовался пример, когда такая зависимость существенно сказывается на теплообмене. [13]
Полученные граничные условия показывают, что коэффициенты каталитической активности поверхности kwo и fcWN в общем случае являются функциями не только температуры, давления и химического состава, но и диффузионных потоков компонентов. В [117] исследовался пример, когда такая зависимость существенно сказывается на теплообмене. Рассматривалось обтекание передней критической точки ионизованным азотом, в условиях, когда в пограничном слое существенно влияние процессов ионизации на переносные свойства, трение и теплообмен. [14]
Влияние радиационного закаливания, ионной бомбардировки и отжига на каталитическую активность поверхностей чистого никеля и платины. [15]
Страницы: 1 2 3