Алкансульфокислота
Cтраница 2
У алкилэфиров алкансульфокислот подобное поглощение наблюдал Симон [ 3 ], отнесший это поглощение за счет природы алкильных радикалов. [16]
В результате образуются алкансульфокислоты. [17]
Гербицидной активностью обладают алкансульфокислоты и их производные. [18]
При алкоголизе хлорангидридов алкансульфокислот в присутствии триэтиламина весь образующийся сульфен присоединяется к спирту с образованием эфира сульфокислоты. [19]
О способах синтеза алкансульфокислот было сказано в разделе об алка-нах. Существенны лишь сульфокислоты высших алканов с 15 и более атомами углерода. Натриевые соли этих кислот RS02CTNa используются в современных моющих средствах и заменяют мыло. [20]
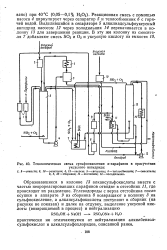 |
Технологическая схема сульфоокисления - парафинов в присутствии. [21] |
Образовавшиеся в колонне 13 алкансульфокислоты вместе с частью непрореагировавших парафинов отводят в отстойник 11, где происходит их разделение. [22]
Найдено [22, 26, 28], что высшие алкансульфокислоты с хорошим выходом могут быть получены окислением соответствующих меркаптанов или дисульфидов в растворе ацетона или уксусной кислоты перманганатом калия, а также двухромовокислым калием. Кислоты выпадают из раствора при действии концентрированной соляной кислоты. [23]
Найдено [22, 26, 28], что высшие алкансульфокислоты с хоро - шим выходом могут быть получены окислением соответствующих меркаптанов или дисульфидов в растворе ацетона или уксусной кислоты перманганатом калия, а также двухромовокислым калием. Кислоты выпадают из раствора при действии концентрированной соляной кислоты. [24]
Основными продуктами после сульфирования и гидролиза являются алкансульфокислоты и гидрооксикислоты. Помимо этих продуктов при гидролизе 1 3 и 1 4 сультонов могут получаться 3 - и 4-гидрооксиалкансульфонаты. Когда сульфирование ведут с комплексообразователем и применяют большой избыток серного ангидрида может образовываться мало растворимый 2-гидрооксиалкансульфонат. [25]
В качестве продуктов при этом получают хлорангидриды алкансульфокислот. [26]
Эти поверхностно-активные вещества представляют собой натриевые соли алкансульфокислот, содержащих от 10 до 18 атомов углерода. [27]
Вещества с общей формулой RSO2C1 представляют собой хлорангидриды алкансульфокислот RSO2OH и называются алкансульфохлори-дами. Они легко гидролизуются до алкансульфокислот, которые являются растворимыми в воде сильными кислотами, подобными серной кислоте. Натриевые соли этих кислот ( алкансульфонаты натрия) RSO3 - Na при соответствующих размерах алкильных групп проявляют свойства, подобные свойствам мыл, и могут применяться в качестве детергентов или других поверхностно-активных агентов. Алкильная группа большого размера придает этим солям липофильные ( жиропо-добные) свойства, а ионная сульфонатная группа гидрофильна. У веществ с алкильной группой, содержащей 10 - 14 атомов углерода, ли-яофильные и гидрофильные свойства сбалансированы таким образом, что эти вещества эмульгируют в воде жиры и масла. [28]
Следует отметить особое значение реакций сульфохлорирования и сульфоокисления для производства алкансульфокислот, имеющих применение в качестве моющих средств. Моющие свойства алкансульфокислот основаны на поверхностной активности молекул этих соединений. [29]
Следует отметить особое значение реакций сульфохлорирования и суль-фоокисления для производства алкансульфокислот, имеющих различное применение, в том числе в качестве моющих средств. Моющие свойства алкансульфокислот основаны на поверхностной активности молекул этих соединений. Имея два фрагмента в своем составе - гидрофобный ( фрагмент алкана) и гидрофильный ( сульфогруппа), молекулы алкансульфокислот приобретают способность ориентироваться на границе раздела фаз, обеспечивая тем самым перенос загрязнений в водную фазу и их удаление с загрязненного материала ( см. разд. [30]
Страницы: 1 2 3 4