Бромидный комплекс
Cтраница 1
Бромидный комплекс менее прочен, чем аммиакат. [1]
Бромидные комплексы с ДМСО не растворимы в ацетоне, хлороформе, бензоле, эфире, растворимы в спиртах, ДМСО и воде. [2]
Бромидный комплекс теллура ( 1У) - желтого цвета, комплекс экстрагируется ТБФ и другими растворителями. Максимум свето-поглощения в ТБФ лежит при 450 нм [1592], окраска устойчива, но избирательность метода невелика. Интересно, что при разбавлении ТБФ толуолом оптическая плотность экстрактов увеличивается: максимальное светопоглощения отвечает 20 % - ному раствору ТБФ. [3]
Бромидные комплексы теллура взаимодействуют с производными пиразолона при 1 5 - 6 М концентрации бромистоводородной кислоты. [5]
Бромидные комплексы кадмия занимают промежуточное положение. [6]
Бромидный комплекс золота окрашен в желто-оранжевый цвет с максимумом поглощения при А, - 380 нм. Этот метод селективен, несложен, но недостаточно чувствителен, поэтому его используют для определения сравнительно больших количеств золота. [7]
Бромидный комплекс индия [ InBrJ образует экстрагируемые бензолом ассоциаты с основными ксантеновыми красителями, родамином В [53, 54], родамином 3В [55] и родамином 6Ж [56, 57], что используется для фотометрического определения индия. [8]
Бромидные комплексы указанных элементов сорбируются ионообменником; для их элюироваиия используют 1 М азотную кислоту. [9]
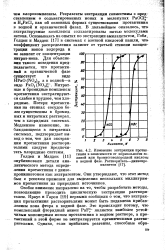 |
Изменение экстракции протактиния в зависимости от нормальности соляной или бромистоводородной кислоты в водной фазе. Растворитель-диизопро-пилкетон. [10] |
Нитратные и бромидные комплексы протактиния экстрагируются слабее и труднее, чем хло-ридные. Потери протактиния на стенках сосудов более существенны в бромид-ных и нитратных растворах, чем в хлоридных системах. Медленное изменение, наблюдающееся в нитратных системах, подтверждает вывод о том, что для экстракции протактиния растворителями следует предпочитать хлоридные системы. [11]
Из окрашенных бромидных комплексов наибольший аналитический интерес представляют соединения золота, теллура и платиновых металлов. Желто-оранжевый комплекс AuBr4 давно применяется для определения золота в различных объектах [1848, 1849]; метод обладает средней чувствительностью. Экстракция из 2 М НВг позволяет отделять золото от платиновых металлов ( кроме Os) и частично от железа. Холбрук и Рейн [224] разработали метод определения золота, основанный на экстракции его из бромидного раствора раствором ТОФО в хлороформе. [12]
Колориметрия бромидного комплекса палладия ( метод мало селективный): G. [13]
Ассоциат аниона бромидного комплекса ртути с катионом родамина С экстрагируется органическими растворителями и флуоресцирует оранжевым цветом [23]; максимум в спектре возбуждения флуоресценции экстракта находится при 560 ммк, максимум излучения - около 590 ммк. [14]
По своей экстракционной способности бромидные комплексы для каждого данного металла располагаются ( за немногими исключениями) между хлоридными и иодидными. В практике экстракции используют извлечение из растворов НВг и не менее часто из смеси бромидов щелочных металлов ( или НВг) с какой-либо минеральной кислотой. Использование таких смесей часто дает существенные преимущества, главным образом для элементов, у которых экстрагируется не высший бромидный комплекс, а промежуточный, и которые склонны к гидролизу. Наиболее характерно это для элементов, способных экстрагироваться инертными растворителями - бензолом, СС14 - в виде координационно насыщенных молекулярных бромидов. [15]
Страницы: 1 2 3 4