Комплексо-образование
Cтраница 1
Комплексо-образование сопровождается сдвигом частоты колебаний связи - С N - на 20 - 25 см-1 в коротковолновую область, частоты валентных колебаний связей Ph - О - и - О - Н не меняются. Это указывает на образование координационных соединений донорно-акцепторного типа, у которых донором электронов является азот азометиновой группировки. Повышение частоты валентных колебаний группы - С N - объяснено усилением поляризации связи. Имеющаяся в основаниях Шиффа внутримолекулярная водородная связь, по-видимому, не претерпевает изменений. [1]
Поэтому комплексо-образование в триоксане может быть обусловлено только донорно-акцепторны М И взаимодействиями типа водородной связи О... Кроме того, в принципе возможны водородные связи, направленные не вверх от одной молекулы к другой, а вбок. [2]
Процесс комплексо-образования протекает медленно: изменение окраски от оранжевой, ( макс 466 ммк) до темно-зеленой ( Ямакс 626 ммк), как и изменение рН, длится более часа. [3]
Использование метода комплексо-образования особенно перспективно, так как прямая перегонка даже в глубоком вакууме остатка, после извлечения терпеновых хлоридов, с целью выделения сесквитерпеновых хлоридов невозможна из-за сильного разложения с выделением хлористого водорода. [4]
Более высокая степень комплексо-образования в случае тория дает основания предполагать, что осаждение тория ( за исключением очень низких плотностей тока) будет происходить за счет вторичного восстановления его литием. В соответствии с этим предположением при электролизе рассматриваемой системы предельный ток отсутствует, а величина потенциала в процессе стационарного осаждения почти равна потенциалу обратимого электрода ( Th Th4 - f - 4e -) при той же концентрации. Поэтому создается впечатление, что имеет место первичное осаждение Th4 1, которое, однако, осуществляется с большей скоростью, чем скорость, определяемая плотностью тока, которую можно получить за счет-ионов Th4 с концентрацией, определяемой константой нестойкости комплекса. [5]
Приведенные выше процессы комплексо-образования можно рассматривать как типичное кислотно-основное взаимодействие с точки зрения электронной теории кислот и оснований Льюиса. С этих позиций ЭГ4 как акцепторы электронной нары выступают в роли кислоты, а лиганды Г, ОН -, являющиеся донорами электронной пары - в качестве основания. [6]
Хорошо известна реакция гетерогенного комплексо-образования с растворением осадка при удалении ржавых пятен с ткани. [7]
Их способность к комплексо-образованию обеспечивается благоприятным расположением атомов серы и азота и зависит от характера замещения у атома кремния и природы сорбируемого металла. [8]
Величины равновесных констант для комплексо-образования Ри4 ( и РиО) с хлорид-ионом ( а также с нитрат-и сульфат-ионами) получены на основании влияния этих анионов на окислительно-восстановительные потенциалы пар. Эта работа выполнена тщательно и подробно. Так как влияние комплексо-образования на величину измеряемого формального потенциала указывает только на различие в устойчивости комплексных ионов, степень связи в комплекс одного из ионов должна быть определена независимым методом. Так было сделано при исследовании ком-плексообразования плутонил-иона с хлоридами. [9]
Спектрофотометрическим методом было исследовано комплексо-образование в системе СеСЬ - 8-оксихинолин - хлороформ с целью определения состава образующегося комплекса. [10]
Ме / Ме2 без комплексо-образования; К аМег Ях / амех - константа комплексообразова-ния; / к и / х - коэффициенты активности; сх - концентрация комплексообразователя; DK и DX - константы диффузии; тх - переходное время для комплексообразователя. [12]
Бондаренко [115-116] полярографически изучил комплексо-образование кадмия с роданид-ионом в водно-этанольных растворах. CCNS - найдено, что в диффузии к капельному электроду участвует несколько видов ионов. [13]
 |
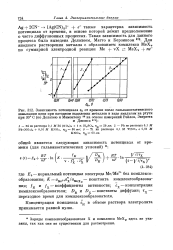
Зависимость концентрации различных комплексных соединений от концентрации лигандов. [14] |
Рассмотрим подробнее двухступенчатый процесс комплексо-образования. [15]
Страницы: 1 2 3 4