Комплексо-образование
Cтраница 2
Проведенное физико-химическое изучение процессов комплексо-образования и сложной динамики равновесных систем [39] и сопоставление полученных результатов с данными исследований биологов и агрохимиков показало, что влияние комплексонов на поведение металлов в почве и растениях в целом определяется устойчивостью их комплексов. [16]
 |
Сорбция ионов меди ( Н из растворов комплексных катионов анионитом АВ-16. [17] |
В этом случае процесс комплексо-образования в фазе ионита аналогичен комплексообра-зованию с гидратированными ( сольватированными) ионами металлов с той лишь разницей, что, во-первых, энергия координационной связи металл - низкомолекулярный лиганд больше энергии связи металл - растворитель, а, во-вторых, побочные реакции, вызывающие образование осадков гидроксидов и основных солей, играют меньшую роль. [18]
Изучение механизма и закономерностей комплексо-образования позволило выявить такие свойства иони-тов, которые дают возможность применять их в самых различных отраслях народного хозяйства. Они широко используются в прогрессивных безотходных производствах, а также для решения многих экологических проблем, связанных с защитой окружающей среды. Возможность практического применения комплекситов определяется состоянием их функциональных групп в системе. При одной и той же химической природе и физической структуре полимера его химические, физико-химические и физические свойства настолько сильно зависят от состояния функциональных групп, что, по существу, они могут рассматриваться как различные виды химически-активных полимеров. Это предопределяет возможность применения разных форм комплекситов для решения многих практически важных задач. [19]
Проведенное физико-химическое изучение процессов комплексо-образования и сложной динамики равновесных систем [39] и сопоставление полученных результатов с данными исследований биологов и агрохимиков показало, что влияние комплексонов на поведение металлов в почве и растениях в целом определяется устойчивостью их комплексов. [20]
Для количественной характеристики процесса комплексо-образования в растворе необходимо определить константу устойчивости образующегося комплекса или константу равновесия соответствующей реакции. [21]
 |
Зависимость степени гидролиза г водного раствора [ Cr ( H2O s ] Cl3 от температуры t ( C. [22] |
Нагревание вызывает уменьшение влияния комплексо-образования на гидролиз, так как константа нестойкости комплексов с повышением температуры увеличивается. [23]
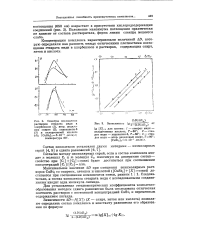 |
Спектры поглощения растворов стеарата меди в хлорбензоле ( 1, втор, децило-вом спирте ( 2, ундеканоне-6 ( 3 и иеларгоновой кислоте ( 4. [ CuSt2 ] o 5 - 10 - 3 молъ / л. температура 60. [24] |
Для установления стехиометрических коэффициентов комплексо-образования методом сдвига равновесия была исследована оптическая плотность растворов с постоянной концентрацией CuSta и переменным содержанием лиганда. [25]
Большинство имеющихся данных по комплексо-образованию плутония ( III) носит в основном качественный характер. В целом тенденция плутония ( III) к образованию комплексных ионов не велика. Некоторые результаты, доказываю-щие существование комплексных ионов ( в концентрированном растворе серной кислоты), получены электромиграционным методом, но в большинстве случаев выводы о комплексообразовании делались на основании спектрофотометрических наблюдений. [26]
Из первых грех фракций комплексо-образованием с Hg2 удаляют сульфиды. Каждую из фракций после удаления сульфидов A lSi4M A2Sl M и выделенные на А1203 фракции A 3S j 4 - Л s Si 4 разделяют на Si02 на четыре подфракции, представляющие собой различные группы соединений, содержащих кислород, азот или оба эти элемента. Последовательное разделение на А1203 и 8Ю2, обладающих разной разделяющей способностью к отдельным классам гетеросоединений, позволяет получить более узкие и химически однородные фракции. Итак, в результате разделения на Si02 получают двадцать подфракции от A1SiM до А 4, отличающихся по своему химическому составу. [27]
Из первых трех фракций комплексо-образованием с Hg2 удаляют сульфиды. Каждую из фракций после удаления сульфидов AiS14 f A Si4AI и выделенные на А12О3 фракции 43 ii - AsSi разделяют на SiO2 на четыре подфракции, представляющие собой различные группы соединений, содержащих кислород, азот или оба эти элемента. Последовательное разделение на А12 О3 и Si02, обладающих разной разделяющей способностью к отдельным классам гетеросоединений, позволяет получить более узкие и химически однородные фракции. Итак, в результате разделения на SiO2 получают двадцать подфракции mA SiM до А 4, отличающихся по своему химическому составу. [28]
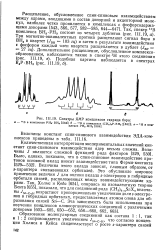 |
Спектры ЯМР комплексов гидрида бора. [29] |
Дополнительное расщепление, обусловленное комплексо-образованием, наблюдается также в спектре гН этого соединения ( рис. III. [30]
Страницы: 1 2 3 4