Комплексоната - металл
Cтраница 1
 |
Константы устойчивости ( lg ( 3 хелатов меди ( П. [1] |
Комплексонаты металлов - частный случай ХКС - используются в количественном анализе для определения катионов различных металлов. [2]
При выборе комплексоната металла для использования в качестве рабочего раствора ( в нашем случае MgY2 -) необходимо соблюдать условие / Сму ( 4) М у2 -, чтобы вытеснительная реакция проходила достаточно полно. [3]
Сопоставляя значения ошибок, вычисленных по уравнениям (4.92) и (4.93), всегда можно найти оптимальный избыток комплексоната замещаемого металла. При значениях q, близких к 1, уравнение (4.92) практически становится тождественным уравнению (4.59), применяемому при обычном прямом титровании, и при этих условиях рекомендации Швар-ценбаха и Флашки [21] справедливы. При 7 1 5 этот коэффициент необходимо учитывать во избежание слишком оптимистических прогнозов. [4]
Особенно велика стабилизация ( рост констант устойчивости Ку до 1025 при координационном числе М2 и М3, равном 6) в комплексонатах металлов. [5]
Возьмем для примера рассмотренные выше условия. Если комплексонат металла характеризуется величиной рЯмет4 ниже этого значения, то степень связывания ионов металла будет еще меньше. [6]
Под условной константой устойчивости комплексоната металла понимают такую характеристику, которая пропорциональна концентрационной константе / ( MY, учитывает влияние рН раствора и дополнительных комплексантов. [7]
Природа химической связи является чрезвычайно сложной и многосторонней проблемой и до настоящего времени содержит ряд необъясненных вопросов. Весьма мало изучена природа химической связи в комплексных соединениях, особенно в полициклических комплексонатах металлов. [8]
 |
Скорость коррозии в конденсате при. [9] |
Многие установки могут одновременно наряду со сталями перлитного и ферритного классов использовать также и другие конструкционные материалы. При наличии в контурах различных конструкционных материалов в воде контура на первом этапе обработки образуются комплексонаты металлов, составляющих основу использованных конструкционных материалов. На втором этапе обработки в соответствии с принципом структурного соответствия разложение комплексонатов происходит при контакте с родственными конструкционными материалами с образованием на каждом из них своих окис-ных защитных пленок. [10]
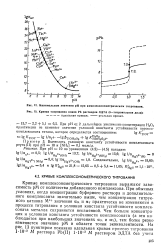 |
Минимальные значения рН при комплексонометрическом титровании.| Кривая титрования ионов РЬ растворов ЭДТА ( в-титровальная доля. [11] |
Кривые комплексонометрического титрования выражают зависимость рМ от количества добавленного комплексона. При обычных условиях, когда концентрации буферного раствора и дополнительного комплексанта значительно выше, чем концентрация титруемого катиона М значения ам и ау практически не изменяются в процессе, титрования и условная константа устойчивости комплексоната металла сохраняется неизменной. Чем больше концентрация и условная константа устойчивости комплексоната ( а это наблюдается при наибольших значениях ам и ау), тем более резко изменяется значение рМ в области точки эквивалентности. [12]
Условия ( 64) будут выполняться практически всегда, если использовать для обратного титрования магний, так как большинство металлов образует более устойчивые комплексы с ЭДТА, чем магний. Поскольку величина константы устойчивости комплекса MgY - не намного больше, чем 107, точка эквивалентности может быть не слишком отчетливой. Чаще всего условия ( 64) оказываются выполненными и в том случае, когда для обратного титрования применяют Мп2 - ионы; в этом случае точка эквивалентности бывает более резкой. Если комплексонат титруемого металла очень устойчив, в роли М могут выступать и многие другие металлы, например цинк и медь, которые пригодны для титрования в кислых растворах. [13]
Вытеснительное титрование применяют в тех же случаях, что и обратное. Вытеснительное титрование может до некоторой степени повысить селективность определения ряда ионов. К раствору определяемого металла прибавляют избыток комплексоната металла определенной концентрации. Обычно применяют комплексонат магния. [14]
Затем бы / и предложены прямые методы со специальными индикаторами - металлохромными или металлометрическими. В начале титрования в растворе индикатор связан в комплекс с определяемым металлом. В конце титрования концентрация ионов металлов уменьшается, потому что комплексонат металла устойчивее комплекса металла с индикатором. [15]
Страницы: 1 2