Арсенит-ион
Cтраница 2
В данном исследовании определялся период полуобмена при различных концентрациях арсенат - и арсенит-иона. [16]
Если предварительно убедиться в отсутствии в исследуемом растворе арсената ( например, по реакции с KJ или с молибдат-ным реактивом), то арсенит-ион легко можно обнаружить после окисления его до арсената любой из описанных ниже реакций на арсенат-ион. [17]
К I группе анионов относятся: сульфат-ион S04, сульфит-ион 5Оз, тиосульфат-ион S 03, карбонат-ион СОз, фосфат-нон РОТ, арсенат-ион AsOi, арсенит-ион АзО, борат-ион ВОТ или В4О7, хромат-ион СгО4, фторид-ион F, силикат-ион ЗЮз и др. Перечисленные анионы образуют с ионами Ва 4 трудно растворимые в воде соли, которые, за исключением BaSO4, растворимы в кислотах. Поэтому анионы I группы не осаждаются из кислых растворов. [18]
В 5 М NaOH, содержащем 60 г / л маннита, анодная полярограмма мышьяка ( Ш) имеет одну резкоочерченную волну [108], пропорциональную концентрации арсенит-иона; при этом определению мышьяка ( Ш) не мешают Cd, Pb, Zn, Bi, Mo, V, W, Cr, Al, Ca, Ba, K, Na, Fe ( III), Sn ( IV), As ( V), Sb ( III), сульфаты, карбонаты, фосфаты и фториды. [19]
Для отделения мышьяка от других элементов используют методы, основанные на ионообменном поглощении сопутствующих элементов, а также методы, основанные на селективной сорбции арсенат - или арсенит-иона анионообменными смолами. [20]
Дробная реакция на арсенит - и арсенат-ионы. Арсенит-ион обнаруживают следующим образом. В полумикропробир-ку помещают 3 капли раствора арсенита натрия и добавляют 5 капель раствора магнезиальной смеси ( смесь гидроокиси аммония и хлорида магния) и 3 капли раствора хлорида аммония. Кристаллический осадок не выпадает. [21]
К 2 - 3 каплям раствора арсенита натрия добавляют немного твердого гидрокарбоната натрия и после его растворения, перемешав раствор, добавляют каплю йодной воды. Аналогично арсенит-ион обесцвечивает бромную воду. [22]
Обнаружению арсенат-иона данной реакцией мешает арсенит-ион, который также в этих условиях образует с сероводородом характерный желтый осадок. Однако арсенит-ион не осаждается магнезиальной смесью. [23]
Потирание стеклянной палочкой о стенки пробирки ускоряет выпадение осадка. С арсенит-ионами эта реакция не идет. [24]
Осадок растворим в кислотах. С арсенит-ионами осадка не образуется. [25]
Почему цепная реакция окисления сульфита кислородом индуцирует окисление арсенита. Очевидно, арсенит-ион, получая удар от какой-нибудь частицы в ходе цепной реакции сульфид - кислород, становится активным и в таком виде легко окисляется. Цепной процесс повышает энергетический уровень арсенит-ионов. [26]
К 2 - 3 каплям испытуемого раствора добавляют немного твердого NaHCO3 и по каплям раствор иода. В присутствии арсенит-ионов иод обесцвечивается. [27]
Если осадок, полученный после действия на раствор магнезиальной смесью ( см. выше), отцентрифугировать, то центрифугат содержит арсенит-ионы, не осаждаемые магнезиальной смесью. Выделение желтого осадка As2Ss указывает на присутствие арсенит-иона. [28]
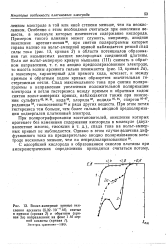 |
Вольт-амперные кривые окисления арсенита ( 5 32 - 10 - 4 М, снятые в прямом ( кривая 2 и обратном ( кривая 2а направлениях на фоне 1 М серной кислоты ( кривая /. Электрод сравнения - НВЭ. [29] |
Особенно с этим необходимо считаться при окислении веществ, в молекуле которых изменяется содержание кислорода. Примером такого влияния может служить, например, анодное окисление арсенит-ионов 89, при снятии полярограммы которых справа налево на вольт-амперной кривой наблюдается резкий спад силы тока ( рис. 13, кривая 2) в области потенциалов образования так называемых высших кислородных соединений платины. Спад максимального тока при снятии полярограммы в направлении увеличения положительной поляризации электрода и петля гистерезиса между прямым и обратным ходом снятия вольт-амперных кривых, наблюдаются также при окислении сульфита62 - 90 91, иода92, хлорида93, иодида 9294, спиртов95 97, роданида 97, тиомочевины98 и ряда других веществ. [30]
Страницы: 1 2 3 4