Диссоциация - реагент
Cтраница 2
Данные спектрофотометрического изучения образующихся форм стильбазо в различных средах послужили основой для определения констант диссоциации реагента. [16]
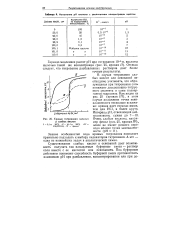 |
Изменение рН кислоты с увеличением концентрации щелочи.| Кривые титров амия сильных и слабых кислот. [17] |
В случае титрования слабых кислот или оснований необходимо учитывать, что образующаяся при титровании соль понижает диссоциацию титруемого реагента и сама подвергается гидролизу. Как ( Видно из рис. 25 ( кривая / / /), в этом случае положение точки эквивалентности несколько искажено: кривая идет гораздо выше, чем для НС1, и более круто. [18]
Атомарный фтор, образующийся из газообразного фтора при нагревании, электрическом разряде, действии ионизирующего излучения или диссоциации фторирующего реагента, легко реагирует с ксеноном. Получены также два фторида криптона KrF2 и KrF4, но эти соединения образуются с большим трудом, чем соединения ксенона. Еще хуже охарактеризован фторид радона RnF4 вследствие ничтожно малых количеств имеющегося радона и в связи с трудностью работы, обусловленной интенсивной радиоактивностью. [19]
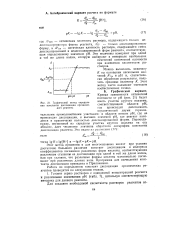 |
Графический метод определе. [20] |
Перпендикуляр, опущенный из середины участка крутого подъема на ось абсцисс, дает численное значение обратного логарифма константы диссоциации реагента. [21]
Другая сторона влияния постороннего электролита состоит в уменьшении диэлектрической проницаемости водной фазы, что приводит к изменению константы диссоциации реагента и константы устойчивости комплекса. Изменяются и константы распределения, которые зависят от ионной силы раствора. Суммарный результат действия солей предсказать довольно трудно. Физическая химия накопила значительный материал о коэффициентах активности неэлектролитов в растворах электролитов [52, 53], но эти данные учитывают не все стороны процессов, протекающих при экстракции внутрикомплекеных соединений. [22]
Согласно уравнению i (4.3), коэффициент распределения DK должен быть прямо пропорционален константе устойчивости комплекса и п-и степени константы диссоциации реагента. Поскольку с уменьшением значения константы диссоциации реагента устойчивость комплекса возрастает, нельзя полагать, что константа устойчивости и константа диссоциации оказывают независимое влияние на коэффициент распределения. [23]
В частности, не рассмотрены особенности протолитического поведения реагента в основном и возбужденном состояниях; не определены надежно константы диссоциации реагента. Не изучен детально состав комплексного соединения. В [7] ему приписывается димерное строение; форма вхождения металла А12 ( ОН), однако исчерпывающих доказательств этого не приводится. Причины высокой контрастности реакции не вскрываются. [24]
Вещества, легко отдающие атомы или молекулы фтора имеют общее преимущество в том, что часть теплоты фторирования расходуе - Рся на диссоциацию реагентов и, таким образом, вся реакция протекает более спокойно. Недостатком этих веществ является то, что они должны регенерироваться, если только реагирующее вещество не является достаточно инертным по отношению к фтору; в Этом случае они могут использоваться в качестве катализаторов-переносчиков. Однако обычно реаги - - рующие вещества не являются инертными. [25]
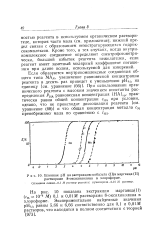 |
Влияние рН на экстракцию кобальта ( П и марганца ( II растворами 8-оксихинолина в хлороформе. [26] |
При использовании органического реагента с высоким значением константы распределения РНА равновесная концентрация ЩА ] орг практически равна общей концентрации снд при условии, однако, что не происходит диссоциации реагента [ см. уравнение ( 68) 1 и что общая концентрация металла см пренебрежимо мала по сравнению с снд. [27]
 |
Зависимость числа Ну.| Зависимость числа Нус. [28] |
Следует отметить, что чем больше Тон, тем менее точной становится постановка задачи о высокотемпературном зг-жигании реагента, так как в этом случае необходимо учитывать сжимаемость реагирующего газа и зависимость тег-лофизических коэффициентов от температуры, а также диссоциацию реагента. Если Г0г0, то зажигания реагента не происходит. [29]
Для ПАН-2 и ТАН-2 показано [211], что независимо от природы растворителя ( диоксан, этанол, ацетон, ДМФА) при его концентрации в растворе 20 - 50 об. % можно вывести единое уравнение, связывающее условную константу диссоциации реагента с диэлектрической проницаемостью раствора. Найденную закономерность нужно учитывать для повышения селективности определения. [30]
Страницы: 1 2 3 4