Диссоциация - гидрат
Cтраница 1
Диссоциация гидрата В ( ОН) 3 в растворе идет по кислотному типу. Однако борная кислота очень слаба и поэтому из растворов своих солей легко выделяется большинством других кислот. Последняя является кислотой значительно более сильной, чем ортоборная. [1]
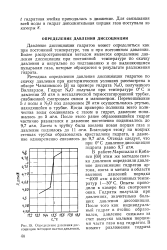 |
Определение давления диссоциации методом скачка давления. [2] |
Давление диссоциации гидратов может определяться как при постоянной температуре, так и при постоянном давлении. Более распространенным методом является определение давления диссоциации при постоянной температуре по скачку давления и визуально по подтаиванию и по выделяющимся пузырькам газа, которые образуются в результате разложения гидрата. [3]
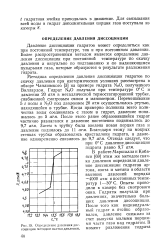 |
Определение давления диссоциации методом скачка давления. [4] |
С давление диссоциации гидрата равно 9 7 атм. [5]
Зная давление диссоциации гидратов и насыщенного пара свободной воды в зависимости от температуры, легко рассчитать энергию связи влаги и соответствующие тепловые эффекты. [6]
К явлениям диссоциации гидратов газов на лед и газ применим закон действующих масс. Стабильность гидратов газов увеличивается с увеличением дипольного момента и молекулярной рефракции газа также и в ряду инертных газов, в котором наиболее реакционноспособным должен быть радон. Из закона действующих масс следует, что в газовой фазе коэффициент гидратации газа при постоянной концентрации водяных паров остается постоянным при уменьшении давления газа. Следовательно, даже при исчезающе малой концентрации радона в газовой фазе часть его атомов должна быть гидратирована. Радон может быть при температуре - 3.5 количественно захвачен твердой фазой 5О2 - гидрата. Радон распределяется между газовой фазой и кристаллическими гидратами SCy6H2O и HS - 6H2O по закону распределения вещества между двумя несмешивающимися фазами. Используя различную реакционную способность в отношении образования гидратов, можно произвести количественное отделение друг от друга элементов нулевой группы чисто химическим путем. [7]
При измерении упругости диссоциации гидратов обычно лучше, когда точка равновесия достигается со стороны меньших давлений, так как при слишком высоком давлении водяного пара на поверхности раздела может установиться ложное равновесие. Причины необратимости полностью не выяснены, но согласно возможной интерпретации ложного равновесия, основывающейся в значительной мере на результатах работы Завадского по карбонатам, при избыточном давлении водяного пара в переходном слое возникает большое число маленьких зародышей первичного гидрата. Благодаря своей малой величине они обладают давлением разложения, превышающим таковое для плоской границы раздела, и дают высокие давления диссоциации. [8]
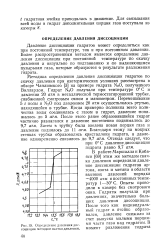 |
Определение давления диссоциации методом скачка давления. [9] |
Методика определения давления диссоциации гидратов по скачку давления при изотермических условиях рассмотрена в обзоре Чаплинского [3] на примере гидрата № 0, полученного Виллардом. [10]
Если известна упругость диссоциации гидрата на газ и лед, так же как парциальное давление паров воды надо льдом и переохлажденной водой ( с поправкой на уменьшение давления паров вследствие растворения хлора), то можно вычислить упругость диссоциации гидрата на газ и воду. [11]
Визуальный метод определения давления диссоциации гидрата при изотермических условиях заключается в следующем. Часть газа над гидратом медленно стравливают малыми порциями. В момент разложения гидрата происходит его подтаивание и выделение пузырьков из гидратной массы до тех пор, пока в ячейке пе будет достигнуто давление, равное давлению диссоциации гидрата. [12]
В первом приближении упругость диссоциации гидрата неона должна отличаться во столько же раз от упругости диссоциации гидрата аргона, во сколько последняя отличается от упругости диссоциации гидрата радона. Константы распределения D в системе гидрат SO2 - инертный газ должны отличаться друг от друга таким же образом. [13]
При нагреве выше температуры диссоциации гидрата окиси кальция ( 547) и последующем увлажнении бетон разрушается из-за гашения свободной извести. При пожарах, однако, бетон показал себя достаточно стойким. Это объясняется его сравнительно малой теплопроводностью, вследствие чего высокие температуры действуют лишь на сравнительно небольшую глубину; внутри же бетон остается холодным, и поэтому прочность его не изменяется. [14]
Применимость закона действующих масс к диссоциации гидратов газов может быть проверена. [15]
Страницы: 1 2 3 4