Диссоциация - гидрат
Cтраница 3
При добавлении щелочи в раствор произойдет обратное: создается большая концентрация ионов ОН, благодаря чему подавляется диссоциация гидрата окиси алюминия по основному типу. Ионы гидроксила щелочи связывают ионы Н, образуя воду. [31]
Абсолютная устойчивость гидрата характеризуется температурой, при которой упругость диссоциации достигает 1 ат, или же упругостью диссоциации гидрата при О С. Б. А. [32]
Таким образом, для вычисления фактора разделения с помощью уравнения (7.6) достаточно располагать надежными численными значениями давлений диссоциации индивидуальных гидратов А и В при данной температуре. В табл. 22 приведены значения Рдисс. [33]
До сих пор гидраты газов получали только одним методом - сжиманием газа над водой, реже надо льдом, до давлений, превышающих упругость диссоциации гидрата при данной температуре. По Форкрану, упругость диссоциации гидрата аргона при 0 составляет 98 атм. Вийяр указывает, что получить гидрат аргона нелегко. Необходимо конец реакционной трубки охладить ниже 0 и вызвать кристаллизацию льда, и лишь тогда начинает выделяться гидрат аргона. [34]
В первом приближении упругость диссоциации гидрата неона должна отличаться во столько же раз от упругости диссоциации гидрата аргона, во сколько последняя отличается от упругости диссоциации гидрата радона. Константы распределения D в системе гидрат SO2 - инертный газ должны отличаться друг от друга таким же образом. [35]
Если известна упругость диссоциации гидрата на газ и лед, так же как парциальное давление паров воды надо льдом и переохлажденной водой ( с поправкой на уменьшение давления паров вследствие растворения хлора), то можно вычислить упругость диссоциации гидрата на газ и воду. [36]
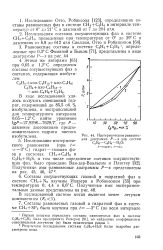 |
Изотермическая равновесная диаграмма Р - х для систем С3Н6 - С3Н8 - Н2О. [37] |
В ходе исследований уда - лось получить смешанный гидрат, содержащий до 85 5 об. % изобутилена, и экстраполяцией для температурного интервала 0 65 - 1 2 С найти уравнение IgP 27 9298 - 7629 / 7, где Р - давление диссоциации предположительного гидрата чистого изобутилена. [38]
Выше мы указывали, что в результате расчета теплоты образования гексааквоманганоиодида, основанного на применении термохимических радиусов ионов, обнаружено серьезное расхождение между теоретически вычисленной величиной ( - ДЯ 298 491 ккал) и полученной Биховским и Россини [31] на основании опытных данных Лекера [84] по измерению упругости диссоциации данного гидрата. [39]
Полярографию применяли главным образом для изучения скорости реакции СН2 ( ОН); чь СН2О - ( - Н2О ( см. раздел IV, В), причем положение равновесия определяли заранее, однако в принципе полярография может быть применена также для определения констант равновесия при условии, что степень диссоциации гидрата небольшая, а скорость диссоциации не слишком высока. Наиболее точный метод состоит в использовании осциллографической полярографии. [40]
Упругость диссоциации соединения достигает 1 ат. Аналогично диссоциации гидратов логарифм упругости диссоциации соединений фенола является линейной функцией от температуры. Как видно из рисунка, логарифмические прямые идут параллельно для всех четырех соединений. Упругости диссоциации двух аналогов в отношении образования молекулярных соединений - H2S и НВг - очень близки, и логарифмы их изменяются параллельно с температурой. Это доказывает однотипность химической связи в обоих соединениях и их одинаковую химическую формулу. Соединение с СО2 образуется только при высоких давлениях. При 0 упругость диссоциации составляет около 1300 мм и достигает 1 ат. Образуют ли инертные газы подобные соединения с фенолом. [41]
Он получается при сжатии арсина в присутствии воды. Давление диссоциации гидрата равно 1 ат при 1 0 С и 17 5 ат при 28 3 С. Выше этой температуры, при соответствующем давлении, гидрат разлагается с образованием двух жидких слоев. [42]
При 0 она должна составлять несколько тысяч атмосфер. Упругость диссоциации гидрата аргона при 0 составляет 98.5 атм. Области давлений в тысячи атмосфер с трудом доступны в лабораторных условиях. Но даже, если бы компримированием неона над водой удалось бы получить гидрат неона, доказать это было бы очень трудно. [43]
 |
Зависимость давления пара свободной воды ( / и связанной воды ( 2 от температуры. [44] |
Различают воду, связанную в виде гидроксильных ионов, и воду молекулярных соединений типа кристаллогидратов, последняя связана значительно слабее первой. По величине давления диссоциации гидратов в зависимости от температуры можно рассчитать свободную энергию связи воды и теплоты нарушения связи, приняв за основу зависимость давления насыщенного пара свободной воды от температуры. [45]
Страницы: 1 2 3 4