Ацетилбензоил
Cтраница 2
Постороннюю окраску компенсируют по контрольному опыту, который ставят со всеми реагентами, кроме ацетилбензоила. [16]
Несмотря на сравнительно высокую температуру реакций, при которой обычно наблюдается диссоциация перекисей бензоила и ацетилбензоила, выделение двуокиси углерода незначительно. [17]
Перекись бензоила, наряду с сокращением индукционного периода, приводит к некоторому повышению максимальной скорости накопления и выхода перекиси ацетилбензоила. Добавки надбензоиной кислоты, сокращая начальный период, вызывают значительное торможение на более глубоких стадиях. Этим и объясняются высокие требования к чистоте исходного бензальдегида, поскольку в противном случае нельзя достичь воспроизводимых и стабильных результатов. Добавки перекиси ацетилбензоила и особенно надбензоиной кислоты ускоряют процессы уплотнения и приводят тем самым к более высокому содержанию смол в конечном продукте. [18]
При суспензионном методе чаще всего употребляют два типа инициаторов полимеризации: перекисные, такие, как перекиси бензоила, ацетилбензоила, ацетила, и непе-рекисные, а именно, азосоединения, например, а, а - азо-оис-изобутиронитрил и др. Более высокой активностью характеризуются перекисные инициаторы; что же касается азосоединений, то их используют для производства цветных сортов суспензионных полимеров, так как в отличие от первых они не оказывают разрушающего действия на красители. [20]
К 1 мл гидролизата прибавляют 1 мл 60 % раствора КОН в 0 2 мл 1 % спиртового раствора свежеприготовленного ацетилбензоила. [21]
При окислении бензальдегида воздухом в присутствии уксусного ангидрида удается задержать реакцию на стадии образования перекиси, причем гидроперекись бензоила превращается о этих условиях в перекись ацетилбензоила. [22]
При окислении бензальдегида воздухом в присутствии уксусного ангидрида удается задержать реакцию на стадии образования перекиси, причем гидроперекись бензоила превращается в этих условиях в перекись ацетилбензоила. [23]
При окислении бензальдегида воздухом в присутствии уксусного ангидрида удается задержать реакцию на стадии образования перекиси, причем гидроперекись бензоила превращается в этих условиях в перекись ацетилбензоила. [24]
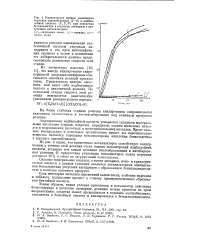 |
Кинетические кривые накопления перекиси ацетилбензоила ( 1 - 3 и надбен-зойной кислоты ( Г, 2, 3 при окислении бензальдегида в уксусном ангидриде в присутствии катализаторов. [25] |
Таким образом, меняя условия проведения и катализатор окисления бензальдегида в уксусном ангидриде, реакцию можно провести по трем направлениям: альдегид может превращаться в перекись ацетилбензоила, окисляться в бензойную кислоту и ацилироваться в бензилидендиацетат. [26]
В рассматриваемой системе расходование надбензойной кислоты ( основного продукта цепного окисления бензальдегида) происходи в основном по двум реакциям: надбензойная кислота ацилируется уксусным ангидридом в перекись ацетилбензоила и надбензойная кислота окисляет бензальдегид в бензойную кислоту. В среде уксусного ангидрида преимущественно протекает первая реакция. [27]
В настоящее время химическая поляризация ядер ( ХПЯ) исследована во многих реакциях термического распада перекисей и азо-соединений, процессах изомеризации с миграцией молекулярных фрагментов и др. На рис. III.17 в качестве примера показано, как выглядит спектр ПМР продуктов, получающихся при термическом распаде перекиси ацетилбензоила в тетрахлорэтилене при 100 С; видны несколько сигналов эмиссии ( направлены вниз), обусловленных отрицательной сверхравновесной ХПЯ. Для каждого пика на рисунке указано его отнесение. Обнаружение эффектов химической поляризации является надежным критерием существования радикальных стадий реакции. [28]
При концентрациях перекиси ацетилбензоила 0 1 молъ / л первый порядок по альдегиду сохраняется, в то время как порядки по перекиси и уксусной кислоте меняются с ростом концентрации перекиси. В интервале концентраций перекиси ацетилбензоила 0 - 0 5 молъ / л практически весь альдегид превращается в перекись. При концентрациях перекиси 0 5 молъ / л скорость ее накопления перестает подчиняться указанному кинетическому уравнению. Здесь же начинает наблюдаться заметное расходование альдегида в другие продукты, в результате чего выход перекиси даже в самых лучших случаях не превышает 80 % от теории. В конечных продуктах реакции были обнаружены в небольших количествах перекись бензоила, бензилидендиацетат, бензойная кислота и продукты уплотнения, Кинетическая кривая накопления надбензойной кислоты имеет максимум, что соответствует представлениям о промежуточном продукте. [29]
Добавки перекиси ацетилбензоила в концентрациях 0 - 0 5 моль / л приводят к сокращению индукционного периода, максимальные скорости накопления перекиси и расходования альдегида практически остаются постоянными. Несильно меняется и выход перекиси ацетилбензоила. [30]
Страницы: 1 2 3 4